��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ3Zn(OH)2+2Fe(OH)3+4KOH 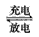 3Zn+2K2FeO4+8H2O��������������ȷ���� [???? ]
3Zn+2K2FeO4+8H2O��������������ȷ���� [???? ]
A���ŵ�ʱÿת��3mol���ӣ�������1mol K2FeO4������
B�����ʱ������ӦΪ��Fe(OH)3 -3e-+5OH-==FeO42- +4H2O
C���ŵ�ʱ������ӦΪ��Zn-2e-+2OH-==Zn(OH)2
D���ŵ�ʱ����������Һ�ļ�����ǿ
�ο��𰸣�A
���������
�����Ѷȣ�һ��
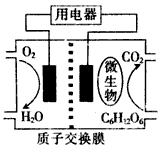
2��ѡ���� ��������Ϊȼ�ϵ�����ȼ�ϵ�ؽṹʾ��ͼ��ͼ��ʾ�����ڸõ�ص�������ȷ����
 [???? ]
[???? ]
A.�õ���ܹ��ڸ����¹���
B.��صĸ�����ӦΪ��C6H12O6+6H2O-24e-=6CO2��+24H+
C.�ŵ�����У�H+������������Ǩ��
D.�ڵ�ط�Ӧ�У�ÿ����1 mol�����������������ɱ�״����CO2���� L
L
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� ����ͭпԭ��غ͵��CuCl2��Һ��װ�ã�����ͼ��������˵����ȷ���ǡ���������??��
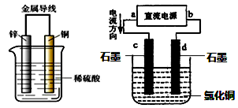
A��п�Ǹ�����ͭƬ�������ݲ�����������пƬ����������ͭƬ
B��ͭƬ�������٣���������ͭƬ���汻��ԭ
C��dΪ�������缫��ӦΪ��2Cl����2e��=Cl2��
D���������У� d�缫��������
�ο��𰸣�D
���������A �����ǵ��Ӵ�пƬ����������ͭƬ
B ����ͭƬ��������
C ����d������Cu2++2e��=Cu
D ��ȷ��ͭ��d�缫�������������ӡ�
�����Ѷȣ�һ��
4��ʵ���� ��Ҫ�����ͼ���������б�Ҫ�����Ӳ���գ�
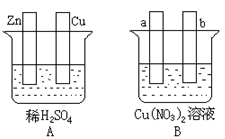
��1����Aͼ�У�ʹͭƬ��ðH2���ݡ�����Ա�Ҫ���ӣ�
�����Ӻ��װ�ý�???????????????��
�缫��Ӧʽ��п�壺????? _______________��
ͭ�壺????????? ___________
��2����Bͼ�У���a��b��Ϊ���Ե缫��
ʹa������ͭ������Ա�Ҫ�����Ӻ�װ�ý�???????????????��
�缫��Ӧʽ��a����??????????????��b����???????����??????��
�ھ���һ��ʱ���ֹͣ��Ӧ��������Һ����Һ��pH????????�����ߡ����͡����䣩������һ������?????��������????����Һ�ָܻ�������ǰ��ȫһ�¡�
�ο��𰸣����ӻ����ԡ���1��ԭ��أ�п�壺Zn-2e- =Zn2��ͭ��
���������
���ӻ��ߣ�����ͼ��
��ԭ��أ�п�壺Zn-2e- =Zn2��ͭ�壺2H2�� ��2e-��H2����2�����أ�a��Ϊ������Cu2����2e- =Cu��b��Ϊ������4OH�D�D4e����O2����2H2O����������HNO3,��ҺPH���ͣ����ɵ�ͭ������������CuO��Һ�ָܻ�������ǰ��ȫһ�¡�

�����Ѷȣ���
5������� ��14�֣�Ǧ�����ǿɳ���͵�أ����������������Ƕ��Բ��ϣ�����ܷ�ӦʽΪ��?
Pb+PbO2+4H++2SO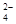
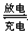 2PbSO4+2H2O
2PbSO4+2H2O
��ش��������⣨�������⡢����������ԭ����?
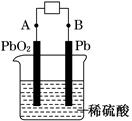
(1) �����طŵ繤��ʱ�ĸ���������????????���������Ȼ�����Һ�����������ռ���11.2L����ʱ������£��������ϸ��������������???????g��
���ʱ����ͼ��A��Ӧ��ֱ����Դ��??????????????(�������������)�����ʱA���ĵ缫��Ӧʽ��????????????????????????????;
(2) MnO2����������֮һ����ʯīΪ�缫������ữ��MnSO4��Һ�������ĵ缫��Ӧʽ����?????�� ��������Ǧ����Ϊ��Դ��⣬����������0.4mol H+������ʱ�����·��ͨ���ĵ��ӵ����ʵ���Ϊ????��MnO2�����۲���Ϊ��?��g��
�ο��𰸣�(1)Ǧ??48��?�� ??PbSO4+2H2O��2e-=
���������
�����������1�����ݵ�ص��ܷ�Ӧ��֪��Ǧ���طŵ�ʱ�ĸ�������������Ӧ�����Ը�������ΪPb�������ĵ缫��ӦΪPb-2e-+SO42-=PbSO4����˸������ӵ�����ΪSO42-���������øõ�ص���Ȼ�����Һʱ�����������ռ�11.2L����ʱ��ת��1mol���ӣ����Ը�������48g�����ʱ��A��Ӧ����������Ӧ���������Դ�����������缫��ӦΪPbSO4+2H2O��2e-= PbO2+4H++SO42-��
��2������ữ��MnSO4��Һ������������ԭ��Ӧ���缫��ӦΪ2H+��2e����H2������Ǧ���ص�
�����Ѷȣ�һ��