微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 汽车的启动电源常用铅蓄电池。下列叙述正确的是 [???? ]
A. 放电时,电子从PbO2一极流入铅板
B. 放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4
C. 充电时,PbO2得到电子,被氧化
D. 放电时,溶液的酸性增强
参考答案:B
本题解析:
本题难度:一般
2、选择题 被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内是离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn + 2MnO2+H2O = ZnO + 2MnO(OH)。下列说法正确的是 [???? ]
A.该电池的正极为锌
B.电池正极反应式为:2MnO2 + 2e-+ 2H2O = 2MnO(OH)+2OH-
C.当0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×1023
D.该电池反应中二氧化锰起催化作用
参考答案:B
本题解析:
本题难度:一般
3、填空题 甲醇是一种优质燃料,可制作燃料电池。
(1)工业上可用下列两种反应制备甲醇:
CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
已知:2H2(g)+ O2(g) = 2H2O(g) ΔH3。则2CO(g)+O2(g) = 2CO2(g) 的反应热
ΔH=_____________(用ΔH1、ΔH2、ΔH3表示)。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH4。
CO(g) + 3H2(g) ΔH4。
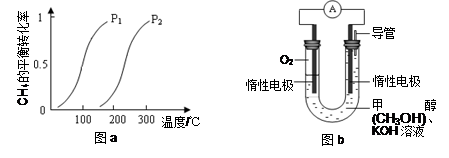
一定条件下CH4的平衡转化率与温度、压强的关系如图a。则ΔH4______0,P1_________P2
(填“<”、“>”或“=”)
(3)某实验小组设计如图b所示的甲醇燃料电池装置,工作一段时间后,溶液的PH (填增大、减小、不变)。负极的电极反应式为_______ ______。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。粗铜电解得到精铜的的电解池中,阳极材料是 ;阴极材料是 ;
阳极泥为:
参考答案:(1)2ΔH1-2ΔH2+Δ
本题解析:
试题分析:(1)根据盖斯定律可知,①×2+③-②×2即达到反应2CO(g)+O2(g)=2CO2(g) ,所以该反应的反应热ΔH=2ΔH1-2ΔH2+ΔH3。
(2)根据图像可知在压强相同的条件下,升高温度甲烷的转化率增大,这说明温度升高平衡向正反应方向移动,所以正方应是吸热反应,即△H大于0;正方应是体积增大的可逆反应,则增大压强平衡向逆反应方向移动,甲烷的转化率降低。所以根据图像可知,在温度相同的条件下,P1对应的转化率高,则P1小于P2。
(3)甲醇在反应中失去电子,所以甲醇在负极通入,电极反应式是CH3OH-6e-+8OH-=CO32-+6H2O,即反应后有碳酸钾生成,消耗氢氧化钾,所以溶液的pH减小。
(4)粗铜精练时,粗铜和电源的正极相连,做阳极,纯铜和电源的负极相连,做阴极。粗铜中的Ag、Au等杂质不失去电子,成为阳极泥。
考点:考查反应热的计算、外界条件对平衡状态的影响、电极反应式的判断和书写阳极粗铜的冶炼
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,综合性强,在注重对学生基础知识巩固与训练的同时,侧重对学生能力的培养与解题方法的指导和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:一般
4、填空题 氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答

(1)氢氧燃料电池的能量转化主要形式是_______________,在导线中电子流动方向为__________(用a、b表示)。
(2)负极反应式为____________________。
(3)电极表面镀铂粉的原因为______________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:?
Ⅰ.2Li+H2 2LiH
2LiH
Ⅱ.LiH+H2O==LiOH+H2↑
①反应Ⅰ中的还原剂是____________,反应Ⅱ中的氧化剂是____________。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
____________。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为___________mol。
参考答案:(1)由化学能转化为电能;由a到b
(2)2H2+4
本题解析:
本题难度:困难
5、选择题 有关铅蓄电池的说法中正确的是
A.该电池充电时的反应是一个自发反应
B.该电池放电过程发生的反应是一个自发反应
C.电池放电时,阳极发生还原反应
D.电池放电时,电解质溶液的PH下降
参考答案:B
本题解析:充电是放电的逆向过程,需要外加电源,所以充电不是自发反应,但放电是一个自发反应。A不正确,B正确。电池放电时,正极发生还原反应,负极发生氧化反应,C不正确。铅蓄电池放电时会消耗硫酸生成硫酸铅,反应式为2PbSO4+2H2O 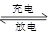 ?Pb+PbO2+2H2SO4,因此溶液的酸性降低,pH增大,D不正确。答案是B。
?Pb+PbO2+2H2SO4,因此溶液的酸性降低,pH增大,D不正确。答案是B。
本题难度:一般