微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中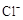 的物质的量浓度之比为 (??? )
的物质的量浓度之比为 (??? )
A.1∶2∶3
B.1∶1∶1
C.3∶2∶1
D.3∶4∶3
参考答案:A
本题解析:
试题分析:根据氯化物的化学式可知,溶液中氯离子的浓度之比是1∶2∶3,而与溶液的体积无关系,答案选A。
点评:该题是基础性试题的考查,难度不大。试题注重基础,兼顾能力的培养。该题的关键是明确构成物质的离子以及相应的电离情况,另外还需要注意的是计算的浓度还是离子的物质的量,有利于培养学生的灵活应变能力。
本题难度:简单
2、选择题 在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为 ( )
A.0.1mol
B.0.5mol
C.0.15mol
D.0.25mol
参考答案:B
本题解析:
试题分析:因溶液中的离子有K+、Cl-、Mg2+、SO42,设SO42-物质的量为n,溶液不显电性,根据电荷守恒:
1.5mol×1+0.5mol×2=1.5mol×1+n×2,解得n=0.5mol.答案选B
考点:物质的量的相关计算
本题难度:一般
3、选择题 下列对物质的量的理解正确的是(??? )
A.物质的量是一种基本物理量
B.物质的量就是物质的质量
C.物质的量就是1 mol物质的质量
D.可以用物质的量来描述苹果
参考答案:A
本题解析:物质的量只适用于微观粒子,如原子、分子、离子、质子、电子及其组合,不适用于宏观物质。
本题难度:简单
4、选择题 10 g 10%的氢氧化钠溶液稀释成50 mL,所得氢氧化钠溶液的物质的量浓度为
A.0.02 mol・L-1
B.0.05 mol・L-1
C.0.25 mol・L-1
D.0.5 mol・L-1
参考答案:D
本题解析:
试题分析:10g10%的氢氧化钠溶液中NaOH的物质的量为10g×10%÷40g/mol="0.025mol," 稀释成50 mL,所得氢氧化钠溶液的物质的量浓度为0.025/0.05="0.5" mol・L-1,选D。
考点:考查物质的量浓度的计算。
本题难度:一般
5、选择题 下列叙述正确的是( )
A.将5.85gNaCl晶体溶入100mL水中,制得0.1mol/L的NaCl溶液
B.将25g无水CuSO4溶于水制成100mL溶液,其浓度为1mol/L
C.将wga%的NaCl溶液蒸发掉
w
2
g水,一定得到2a%的NaCl溶液
D.将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L
参考答案:A、5.85gNaCl晶体的物质的量是0.1mol,将5.8
本题解析:
本题难度:一般
|