��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��NA��ʾ����٤����������ֵ������˵������ȷ���ǣ�??��
A��1 L1mol/L H2SO4������2NA��H+
B��500mL2mol/L�����100mL2mol/L����ĵ�����ǿ
C��1mol Na2S2����NA�����ۼ�
D����״���£�3��36 LSO2������ԼΪ9��6g
�ο��𰸣�B
���������
���������An(H+)=2n(H2SO4)=2��1L��1mol/L=2mol��N(H+)=2NA ��ȷ��B��Һ�ĵ�����������Ũ�ȵĴ�С�йأ�����100mL2mol/L�����500mL2mol/L��������Ũ�ȴ��䵼����ǿ����ȷ��C��S2-�к�����˫����1molNa2S2����2NA�����ۼ�������Dm(SO2)=n��M=��V�MVm����M=(3��36L��22��4L/mol)��64g�Mmol=9��6g,��ȷ��
�����Ѷȣ�һ��
2��ѡ���� NA��ʾ�����ӵ�������ֵ��������������ȷ���� �� ��
A��6.8g���ڵ�KHSO4�к���0.1NA��������
B��1mol�ǻ�������������1mol OH�������������� NA��
C��2L 0.5mol/L�Ĵ�����Һ�к���CH3COO��NA��
D��2g�����������NA������
�ο��𰸣�B
���������6.8g���ڵ�KHSO4Ϊ0.05mol������0.2NA�������ӣ�����
1mol�ǻ�����������Ϊ9 NA����1mol OH������������Ϊ10 NA����B��ȷ������Ϊ������ʲ��ֵ��룬C����2g���������к���4/3NA�����ӡ�
�����Ѷȣ�һ��
3������� ��8�֣�����m gij���壬������˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM g��mol-1���������ӵ���������ֵ��NA��ʾ����
��1������������ʵ���Ϊ????????mol��?
��2������������ԭ������Ϊ????????????����
��3��������������1Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ??????????????��
��4��������������1Lˮ��������Һ���ܶ�Ϊ�� g��cm-3�������ʵ���Ũ��Ϊ???????mol/L��
�ο��𰸣���1��m/M?��2��2 mNA/M??��3��m/��m��100
����������������ʵ������йؼ��㡣
��1������n��m/M��֪������������ʵ�����m/M mol��
��2������������2��ԭ�ӹ��ɵģ�����ԭ�ӵ����ʵ�����2m/M mol�����Ժ��е�ԭ��������2 mNA/M������
��3��1Lˮ������ˮ1000g�������Һ�������ǣ�1000��m��g���������ʵ�����������
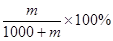
�����Ѷȣ�һ��
4��ʵ���� ��5�֣�����������Ϊ98%���ܶ�Ϊ1.84g/cm3��Ũ��������100mL1.84mol/L��ϡ���ᣬ��ʵ�������У�
A��100mL��Ͳ
B��������ƽ
C��������
D��50mL����ƿ
E��10mL��Ͳ F����ͷ�ι�
G��50mL�ձ� H��100mL����ƿ
ʵ��ʱӦѡ���������Ⱥ�˳���ǣ������ţ��� ��
�ο��𰸣�EFGCHF
���������Ũ��������ϡ���ᣬ����Ҫ��ȡ��Ũ����������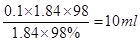 ������������ҪE��F��Ũ�����ϡ�����ձ��н��У�ͬʱ����Ҫ��������ת��ʱͨ��������ת�Ƶ�����ƿ�У�����ݻ���Ҫ��ͷ�ιܣ�����ȷ�Ĵ���EFGCHF��
������������ҪE��F��Ũ�����ϡ�����ձ��н��У�ͬʱ����Ҫ��������ת��ʱͨ��������ת�Ƶ�����ƿ�У�����ݻ���Ҫ��ͷ�ιܣ�����ȷ�Ĵ���EFGCHF��
�����Ѷȣ�һ��
5������� 20 ��ʱ��20 mL NaCl������Һ����Ϊ24 g���������ɺ��ʳ��6.34 g����20 ��ʱ��ʳ�ε��ܽ��Ϊ__________����ʱʳ�ε���������Ϊ__________�����ʵ���Ũ��Ϊ__________��
�ο��𰸣�35.9 g��26.4%��5.42 mol��L-1
���������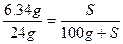 ��S="35.9" g��
��S="35.9" g��
w=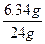 ��100%=26.4%��
��100%=26.4%��
c= �����Ѷȣ���
�����Ѷȣ���