微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 25℃时,在25 mL 0.1 mol・L-1的NaOH溶液中,逐滴加入0.2 mol・Lˉ1的CH3COOH溶液。溶液pH的变化曲线如图所示。下列分析的结论中,不正确的是
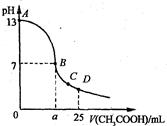
A、C点时c(CH3COO-)>c(Na+)>c(H+)>c(OH―)
B、D点时c(CH3COO-)+c(CH3COOH)=2c(Na+)
C、曲线上A、B间任一点,溶液中都有:c(Na+)>c(CH3COOˉ)>c(OH-)>c(H+)
D、B点的横坐标a=12.5ml
参考答案:D
本题解析:
试题分析:根据电荷守恒,c(CH3COO-)+c(OH―)=c(Na+)+c(H+),C点溶液呈酸性,所以c(CH3COO-)>c(Na+)>c(H+)>c(OH―),故A正确;D点时c(CH3COO-)+c(CH3COOH)=2c(Na+),符合物料守恒,故B正确;当加入及少量醋酸时,c(OH-)>c(CH3COOˉ),故C错误;a=12.5ml时,氢氧化钠和醋酸恰好完全反应,此时溶液呈碱性,故D错误。
考点:本题考查化中和滴定。
本题难度:一般
2、选择题 下列过程或现象与盐类水解无关的是[???? ]
A.纯碱溶液去油污
B.铁在潮湿的环境下生锈
C.加热氯化铁溶液颜色变深
D.浓硫化钠溶液有臭味
参考答案:B
本题解析:
本题难度:简单
3、选择题 氯化铵晶体溶于重水(D2O)中,溶液呈现酸性,下列叙述的原因中正确的是( )
A.NH4+水解生成NH3・H2O和HD2O+
B.NH4+水解生成NH3・DHO和HD2O+
C.NH4+水解生成NH3・D2O和HD2O+
D.NH4+水解生成NH3・DHO和D3O+
参考答案:D
本题解析:氯化铵是强酸弱碱盐,NH4+水解显酸性。水解的实质是NH4+结合水电离出的OH-生成一水合氨,在重水中则结合OD-生成NH3・DHO。在重水中氢离子是以D3O+形式存在。所以正确的答案是D。
本题难度:困难
4、选择题 室温下,下列溶液的离子浓度关系正确的是
A.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
B.NaHSO4溶液:c(H+)=c(SO42-)十c(OH-)
C.Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
D.pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-)
参考答案:B
本题解析:
试题分析:A、混合后溶液中存在电荷守恒为:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-) +2c( C2O42-), A错误;B、根据NaHSO4溶液中的电荷守恒得:c(H+)+c(Na+)=c(OH-)+2c(SO42-),根据物料守恒得c(Na+)= c(SO42-),所以得c(H+)= c(OH-)+c(SO42-), B正确;C、Na2S溶液中,S2-第一步水解生成HS-,S2-两步水解都生成OH-,所以c(HS-) <c(OH-),C错误;D、由于氨水是弱碱,部分电离,氯化氢是强电解质,常温下,pH=2的盐酸溶液浓度小于pH=12的氨水浓度,二者等体积混合,氨水过量导致溶液呈碱性,则c(NH4+)>c(OH-)>c(H+),D错误。答案选B。
考点:考查电解质溶液中离子浓度大小比较,电荷守恒、物料守恒的应用。
本题难度:一般
5、选择题 下列有关电解质溶液中粒子浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
C.pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中:c(NH4+)大小顺序:①>②>③
D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
参考答案:A
本题解析:
试题分析:A.pH=1的NaHSO4溶液中根据电荷守恒c(Na+)+c(H+)=2c(SO42-)+c(OH-)以及物料守恒c(Na+)=c(SO42-)可知c(H+)=c(SO42-)+c(OH-),A正确;B.碘化银的溶度积常数小于氯化银的,则含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)>c(I-),B错误;C.铵跟水解溶液显酸性,氢离子抑制铵跟的水解,则pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中:c(NH4+)大小顺序:①=②>③,C错误;D.含等物质的量的NaHC2O4和Na2C2O4的溶液中根据物料守恒可知2c(Na+)=3[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)],D错误,答案选A。
考点:考查溶液中离子浓度大小比较
本题难度:一般