微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将铝粉与某铁的氧化物FeO?2Fe2O3粉末配制成铝热剂,分成两等份.一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为7.84L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
A.5.6L
B.7.84L
C.11.2L
D.15.68L
参考答案:A
本题解析:分析:分成两等份.一份直接放入足量的烧碱溶液中,只有铝与氢氧化钠发生反应生成氢气,7.84L为氢气体积,根据氢气的体积计算出铝的物质的量.另一份在高温下恰好反应完全,实质为铝置换出铁,铁的氧化物FeO?2Fe2O3中的氧原子全部与铝结合生成氧化铝,利用氧原子守恒,根据铝的物质的量,计算出氧原子的物质的量,再结合氧化物FeO?2Fe2O3的化学式计算出其物质的量,再根据铁原子守恒,可知生成的铁的物质的量.根据铁的物质的量计算铁与盐酸反应生成的氢气体积.
解答:一份直接放入足量的烧碱溶液中,铝与氢氧化钠发生反应生成氢气7.84L,
氢气的物质的量为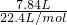 =0.35mol.
=0.35mol.
铁的氧化物FeO?2Fe2O3中的氧原子全部与铝结合生成氧化铝,
所以根据关系式3H2~~~~2Al~~~~3O~~~~Al2O3
?????????????3??????????2???????? 3
????????? ??0.35mol??? 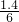 mol????0.35mol
mol????0.35mol
由于氧化物为FeO?2Fe2O3,根据氧原子守恒,所以氧化物FeO?2Fe2O3的为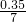 =0.05mol.
=0.05mol.
根据铁原子守恒,可知另一份生成的铁的物质的量为0.05mol×5=0.25mol.
根据Fe~H2可知,0.25molFe可生成氢气0.25mol,所以另一份生成的氢气的体积为0.25mol×22.4L/mol=5.6L.
故选A.
点评:本题考查混合物的计算、铝的性质,题目难度较大,关键清楚反应过程.本解法在反应的基础上利用原子守恒,简化计算步骤,注意守恒思想的灵活运用.
本题难度:困难
2、选择题 某玻璃中含Na2O、CaO、SiO2的质量比约为10:9:58,则此玻璃的组成为
A.Na2O?CaO?6H2SiO3
B.Na2O?CaO?6SiO2
C.2Na2O?2CaO?9SiO2
D.6Na2O?6CaO?SiO2
参考答案:B
本题解析:分析:玻璃的主要成分是硅酸盐,其组成元素可以用元素对应的氧化物来表示,根据氧化物的质量比可以计算元素的原子个数比,进而确定玻璃的组成.
解答:Na2O、CaO、SiO2的质量比约为10:9:58,则Na、Ca、Si的物质的量之比为:( ×2):
×2):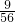 :
: ≈0.32:0.16:0.96=2:1:6,所以氧化物组成为:Na2O?CaO?6SiO2.
≈0.32:0.16:0.96=2:1:6,所以氧化物组成为:Na2O?CaO?6SiO2.
故选B.
点评:玻璃的主要成分是硅酸盐,可以写成氧化物的形式,可以根据元素守恒来确定原子的数目.
本题难度:困难
3、选择题 实验室中为了妥善保存硫酸亚铁溶液常加入少量的
A.镁粉
B.锌粒
C.铁片
D.铜片
参考答案:C
本题解析:Fe可将氧化反应生成的Fe3+还原为Fe2+,其他三种金属虽然也能将Fe3+还原为Fe2+,但又介入了新杂质离子.
本题难度:简单
4、选择题 高锰酸钾是一种典型的强氧化剂.在用KMnO4酸性溶液处理Cu2S固体时,发生如下反应: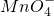 +Cu2S+H+=Cu2++SO2+Mn2++H2O(未配平).下列说法正确的是
+Cu2S+H+=Cu2++SO2+Mn2++H2O(未配平).下列说法正确的是
A.被氧化的元素只有S
B.是氧化剂,既Cu2S是氧化剂又是还原剂
C.氧化性的强弱关系是:
D.生成2.24L片(标况下)SO2时反应中转移电子的物质的量是0.8mol
参考答案:D
本题解析:分析:A、分析反应中元素化合价变化,化合价升高的元素被氧化;
B、依据元素化合价变化判断,元素化合价升高的物质做还原剂,元素化合价降低的物质做氧化剂;
C、氧化还原反应中氧化剂的氧化性大于氧化产物;
D、依据电子守恒计算.
解答:A、反应中铜元素化合价从+1价升高到+2价,硫元素化合价从-2价升高到+4价,化合价升高的元素被氧化,所以被氧化的元素有S、Cu,故A错误;
B、依据化合价变化,锰元素化合价降低,高猛酸钾做氧化剂,Cu2S元素化合价都升高做还原剂,故B错误;
C、氧化还原反应中氧化剂的氧化性大于氧化产物;所以氧化剂MnO4-的氧化性大于氧化产物Cu2+;Mn2+的氧化性小于铜离子,故C错误;
D、生成2.24LL(标况下)SO2时,物质的量为0.1mol;反应的Cu2S物质的量为0.1mol,反应中转移电子的物质的量是:
Cu+~Cu2+~e-;????? S2-~SO2~6e-;0.8mol
1???? ??? 1???????? 1????????6
0.2mol?? 0.2mol????0.1mol???0.6mol?
所以电子转移共0.8mol;
故D正确;
故选D.
点评:本题考查了氧化还原反应的概念分析判断,电子转移计算应用,关键是化合价变化的分析和规律的应用,题目难度中等.
本题难度:困难
5、选择题 由CO、H2和O2组成的混合气体,在一定条件下恰好完全反应,测得生成物在101?kPa、120℃下对空气的相对密度为1.293,则原混合气体中CO所占体积分数为
A.1/3
B.2/3
C.1/2
D.1/6
参考答案:C
本题解析:
本题难度:一般