微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 试样A是由氧化铁和氧化铜组成.取质量相等的两份试样按下图进行实验,最后得到不溶物F和溶液G,不溶物F加入盐酸能放出气体.

(1)写出反应①中氧化铁与铝粉反应的反应方程式:______.
(2)溶液G中的溶质是______.
(3)写出反应②有关的两个离子方程式:______;______.
参考答案:依据流程图分析可知,试样A为氧化铜和氧化铁,加入过量铝粉高温
本题解析:
本题难度:一般
2、选择题 下列说法错误的是
A.仅用KSCN可以检验Fe2+
B.可以用NaOH溶液检验Fe3+
C.通过化合反应可以得到Fe(OH)3
D.通过化合反应可以得到FeCl2
参考答案:A
本题解析:
试题分析:A、KSCN溶液与氯化亚铁混合没有实验现象,要检验亚铁离子,还需要氧化剂例如氯气等,A不正确;B、氢氧化钠溶液与铁离子反应生成红褐色沉淀氢氧化铁,可以检验铁离子,B正确;C、氢氧化亚铁与氧气、水发生化合反应生成氢氧化铁,C正确;D、氯化铁与铁发生化合反应生成氯化亚铁,D正确,答案选A。
本题难度:简单
3、选择题 某同学设计如下实验测量m g铜银合金样品中铜的质量分数:
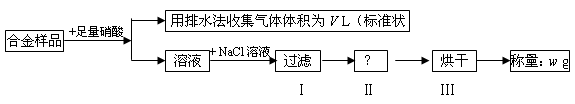
下列说法中不正确的是
A.收集到的V L气体为 NO
B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒
C.操作Ⅱ应是洗涤
D.铜的质量分数为: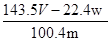 ×100%
×100%
参考答案:D
本题解析:铜和银与硝酸反应,生成NO2或NO,但通过排水法收集到的气体是NO。溶液中加入氯化钠生成氯化银沉淀,即氯化银的质量是wg。所以根据原子守恒可知,合金中银的质量是 ,则铜的质量分数为
,则铜的质量分数为
本题难度:一般
4、选择题 将铝片投入硫酸铜溶液中,会出现下列现象:铝片表面立刻有紫红色物质沉积,同时产生较多气泡,继而产生蓝色沉淀,混合物温度升高甚至发烫,产生气泡速率明显加快,铝片上下翻滚,溶液中出现黑色物质……。对以上现象的说法错误的是(??? )
A.铝片表面的紫红色沉积物为Cu ,离子方程式为2Al+3Cu2+=3Cu+2Al3+
B.生成的气体是H2,生成的蓝色沉淀为Cu(OH)2,产生该现象的离子方程式为3Cu2++6H2O+2Al=3Cu(OH)2↓+3H2↑+2Al3+
C.一段时间后反应速率明显加快的原因一定是;反应放热,使溶液温度升高,反应速率加快
D.溶液中出现的黑色物质可能是氧化铜
参考答案:C
本题解析:铝比铜活泼,和硫酸铜可发生置换反应生成铜,A正确。进而构成原电池,铝是负极加快反应速率,氢离子在正极放电,所以选项C是错误的。反应放热,有可能使氢氧化铜分解生成氧化铜,所以答案选C。
本题难度:一般
5、选择题 下列现象或事实可用同一原理解释的是
A.铁在冷的浓硫酸中和铝在冷的浓硝酸中都没有明显变化
B.浓硫酸和浓盐酸长期暴露在空气中浓度降低
C.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色
D.漂白粉和水玻璃长期暴露在空气中变质
参考答案:A
本题解析:
试题分析:A.铁在冷的浓硫酸中和铝在冷的浓硝酸中都没有明显变化,都是金属铁和铝的钝化现象;B.浓硫酸和浓盐酸长期暴露在空气中浓度降低,前者是吸水,后者是挥发,原理不同;C.使红墨水褪色SO2是化合反应,漂白粉、过氧化钠是氧化,活性炭是吸附;D.长期暴露在空气中:漂白粉是吸潮后与CO2生成HClO,然后分解而变质;水玻璃是直接与CO2反应生成Na2CO3和硅酸而变质。
本题难度:一般