微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题  为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
方案Ⅰ:铜铝混合物??????????????测定生成气体的体积
?
方案Ⅱ:铜铝混合物??????????????测定剩余固体的质量
回答下列问题:
⑴小组成员一致认为两个方案都可行,你认为在实验室中选择方案???????更便于实施。
⑵小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是?????????????????。(填编号)
A.稀盐酸??????? B.氢氧化钠溶液??????? C.硫酸铜溶液
⑶小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45mL时Al3+开始反应生成成沉淀,当加至溶液的体积为50mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
【查阅资料】:常温下Ksp[Al(OH)3]=1.0×10-33mol・L-4,Ksp[Cu(OH)2]=2.0×10-20mol・L-3。
①Al(OH)3开始析出时溶液的PH值?
②若溶液中离子的浓度约为1.0×10-5 mol・L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
2、实验题 某校化学兴趣小组为探究铁与浓硫酸的反应,设计了图1、图2所示装置进行实验。
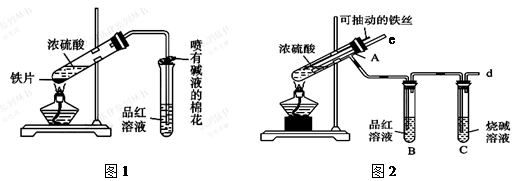
(1)能说明有SO2气体产生的实验现象是?????????????????????????????????。
(2)图2中导气管e的主要作用为?????????????????????????????????????????????。
(3)上述装置中图2中的NaOH溶液能吸收SO2尾气,防止污染,如将其更换为酸性KMnO4溶液,同样可以达到目的,试写出酸性KMnO4溶液与SO2反应的化学方程式:
????????????????????????????????????????????????????????。
(4)对比两套实验装置,不难发现图2装置除了能更好的吸收有毒气体SO2防止其污染环境外,还有一个非常明显的优点,你认为是????????????????????????????????。
(5)反应一段时间后停止反应,待冷却后用胶头滴管吸取A试管中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;???Ⅲ:既有Fe3+又有Fe2+。
为确认溶液的成分,选用如下试剂:
A.稀HCl溶液
B.稀硫酸
C.KSCN溶液
D.酸性KMnO4溶液
E.NaOH溶液???? F.H2O2溶液
试完成下列相关的实验探究:
?
实验步骤
| ?
实验现象及结论
| 1、取一支洁净的试管,滴加1-2mL的试样溶液,再向试管中滴加几滴KSCN溶液
| (1) ????????????????????????,则说明Ⅱ成立。
(2) ????????????????????????,则说明溶液中存在Fe3+,则Ⅰ或Ⅲ成立。
| 2、????????????????????
?????????????????????
| ?????????????????????????????????????????????
????????????????????????????????????????????。
?
3、填空题 下图中的每一方格表示有关的一种反应物或生成物,其中粗框表示初始反应物(反应时加入或生成的水,以及生成沉淀J时的其它产物均已略去)。
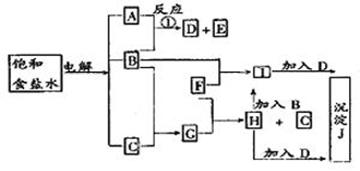
填写下列空白:
(1)物质B是?????,F是?????,J是?????。
(2)反应①的离子方程式是??????
4、实验题 (16分)钢铁工业是国家工业的基础,是日常生活中用途最广、用量最大的金属材料。
(1)常温下,可用铁质容器盛装浓硫酸的原因是??????????????。
(2)在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6mol/L盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
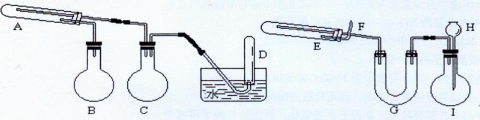
填写下列空白:
①实验进行时试管A中应加入的试剂是????????????;烧瓶B的作用是????????????;烧瓶C的作用是????????????????????。
②实验时,U型管G中加入的试剂是????????????;长颈漏斗H中应加入???????。
③试管E中发生反应的化学方程式是??????????????。
④为了安全,在E管中的反应发生前,在F出口处必须???????????。
5、填空题 将铁与氧化铁的混合物15g加入150mL稀硫酸中,在标准状况下生成1.68LH2,同时固体物质全部溶解,向溶液中加入KSCN溶液,未见颜色改变。为中和过量的硫酸且使铁全部转化为Fe(OH)2,共消耗3mol/LNaOH溶液200mL,则原硫酸溶液物质的量浓度为?? (??? )
A.2mol/L
B.1.8mol/L
C.4mol/L
D.2.2mol/L
|
|