微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知二氯化二硫(S2Cl2)的结构式为Cl―S―S―Cl,它易与水反应2S2Cl2+2H2O→4HCl+SO2↑+3S↓。在该反应中
A.S2Cl2既作氧化剂又作还原剂
B.氧化产物与还原产物物质的量比为3:1
C.每生成22.4L SO2转移3mol电子
D.每生成48g硫会断裂6mol共价键
参考答案:A
本题解析:
试题分析:A. 由二氯化二硫(S2Cl2)的结构式为Cl―S―S―Cl可知,其中的S的化合价为+1价,在反应后的生成物SO2中化合价为+4价,化合价升高,失去电子,作还原剂;在S单质中化合价为0价,化合价降低,得到电子,作氧化剂。因此S2Cl2既作氧化剂又作还原剂。正确。B. 根据方程式2S2Cl2+ 2H2O=4HCl+SO2↑+3S↓可知氧化产物SO2与还原产物S的物质的量的比为1:3。错误。C.每生成1molSO2转移3mol电子。但1mol SO2的体积只有在标准状况下才可能为22.4L。
本题难度:一般
2、填空题 A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大。已知A的一种核素的质量数等于其质子数;E原子最外层电子数为其电子层数的两倍,C、E是同主族元素;B的第一电离能大于C的第一电离能;D离子在同周期离子中半径最小。G的最外层电子排布图为 ,其余各能层电子全充满。
,其余各能层电子全充满。
(1)画出B原子的结构示意图____,G+离子的电子排布式为_____。
(2)C与E组成的一种化合物具有漂白性,该化合物分子中中心原子的VSEPR构型为???。
(3)D单质具有良好导热性的原因是____。
(4)E、F的最高价氧化物对应的水化物的酸性强弱比较(填写化学式):_____>_____。
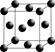
(5)G单质的晶胞结构如图所示,则一个晶胞中G的原子个数为_____。
(6)A与B形成的10电子阳离子在重水中的水解离子方程式为____。
参考答案:(1) 本题解析:
本题解析:
试题分析:由题目提供的信息可知A为H;B为N;C为O;D为Al ; E 为S;F为Cl;G为Cu。(1)N原子的结构示意图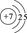 。Cu+离子的电子排布式为1s22s22p63s23p63d10;(2)SO2具有漂白性,该化合物分子中中心原子的VSEPR构型为平面三角形。(3)金属Al是由Al3+和自由电子构成
。Cu+离子的电子排布式为1s22s22p63s23p63d10;(2)SO2具有漂白性,该化合物分子中中心原子的VSEPR构型为平面三角形。(3)金属Al是由Al3+和自由电子构成
本题难度:一般
3、填空题 A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,除G外均为前20号元素。A原子基态时p能级原子轨道上电子数等于次外能层电子数,C元素的原子基态时s能级与p能级上的电子数相等,C、D处于相同的能级,且D是同期中电负性最大的元素,E原子的第一至第四电离能(kJ・mol-1)分别为:578、1817、2745、11575,F元素原子中4s能级有2个电子。G元素的离子形成的硫酸盐结晶水合物呈蓝色。
(1)B形成的单质中σ键和Π键的个数比为????????,上述元素形成的化合物中和B的单质是等电子体的是__________(填化学式)
(2)G元素的基态原子的电子排布式为 。
(3)常温下,E单质投入到B的最高价氧化物对应的水化物的浓溶液中的现象是 。
(4)D、F组成的晶体FD2结构如图Ⅰ所示,G形成晶体的结构如Ⅲ所示,Ⅱ为H3BO3(硼酸)晶体结构图(层状结构,层内的H3BO3分子通过氢键结合)。
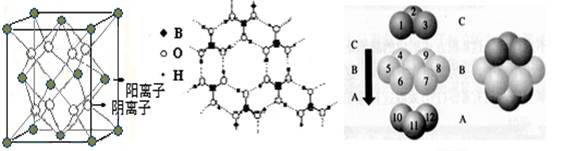
图Ⅰ???????? ??????????图Ⅱ??????? ??????????图Ⅲ
①图Ⅰ所示的FD2晶体中与F离子最近且等距离的F离子数为????????????,图Ⅲ中未标号的G原子形成晶体后周围最紧邻的G原子数为???????????????????;
②图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是???????? (写元素符号),H3BO3晶体中B原子个数与极性键个数比为????????????;
③三种晶体中熔点高低的顺序为????????????????? ?(填化学式),H3BO3晶体受热熔化时,克服的微粒之间的相互作用为??????????????????????????。
参考答案:(1)1 :2??? CO?(2)1s22s22p63s23
本题解析:
试题分析:A原子基态时p能级原子轨道上电子数等于次外能层电子数,且A的原子序数最小,所以A是碳元素。C元素的原子基态时s能级与p能级上的电子数相等,则C是氧元素。由于B的原子序数介于A和C之间,则B是氮元素。C、D处于相同的能级,且D是同期中电负性最大的元素,因此D是F元素。E原子的第一至第四电离能(kJ・mol-1)分别为:578、1817、2745、11575,这说明E位于第ⅢA族元素,因此根据原子序数的大小可知,E应该是Al元素。F元素原子中4s能级有2个电子,且F的原子序数不超过20,所以
本题难度:一般
4、选择题 固体熔化时,必须破坏非极性共价键的是[???? ]
A.冰
B.晶体硅
C.溴
D.二氧化硅
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列化学用语书写正确的是( )
A.乙醇的结构简式:C2H5OH
B.氯化钠的电子式: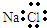
C.S2-离子的结构示意图: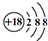
D.有8个质子、10个中子的核素:
168
O
参考答案:A.乙醇含有-OH官能团,乙醇的结构简式:C2H5OH,故A
本题解析:
本题难度:简单