微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率最接近于
[???? ]
A.33%
B.40%
C.50%
D.65%
2、选择题 在密闭容器中的一定量混合气体发生反应: 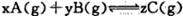 平衡时测得A的浓度为0. 5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时A的浓度变为0. 3m ol/L。下列有关判断正确的是
平衡时测得A的浓度为0. 5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时A的浓度变为0. 3m ol/L。下列有关判断正确的是
A.B的转化率降低
B.x+y<z
C.平衡向正反应方向移动
D.C的体积分数增大
3、填空题 (1)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。
根据题意和所给图像完成下列各题:

①反应达到平衡时,平衡常数表达式K=________。
②升高温度,K值________(填“增大”、“减小”或“不变”)。
(2)一定温度下,将3 mol A气体和1 mol B气体通入一密闭容器中,发生如下反应:3A(g)+B(g)??xC(g)。若容器体积固定为2 L,反应2 min时测得剩余0.6 mol B,C的浓度为0.4 mol・L-1。
请填写下列空白:
①x=________。
②平衡混合物中,C的体积分数为50%,则B的转化率是______________。
4、选择题 .能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的措施是????????????????????
A.将水加热煮沸,测得pH=6
B.向纯水中投入一小块金属钠
C.向水中加入NH4Cl固体
D.向水中加入Na2CO3固体
5、填空题 (16分)化学学科中的平衡理论主要内 容包括:化学平衡、电离平衡、水解平衡和
容包括:化学平衡、电离平衡、水解平衡和
溶解平衡等四种,且均符合勒夏特列原理。请回答下列问题:
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应
A(g)+2B(g)  4C(g)?△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g)?△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
=4mol/L。试确定B的起始浓度c(B)的取值范围是??????????????????????????;若改变
条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是?????????????????。
①增加C的物质的量②加压???③升温④使用催化剂
(2)反应C(s)+CO (g)
(g)  2CO(g)平衡常数K的表达式为?????????????????;
2CO(g)平衡常数K的表达式为?????????????????;
已知C(s)+H 0(g)t
0(g)t CO(g)+H
CO(g)+H ?(g)的平衡常数为K1;H
?(g)的平衡常数为K1;H (g)+CO
(g)+CO (g)
(g)  C0(g)
C0(g)
+H 0(g)的平衡常数为恐,则K
0(g)的平衡常数为恐,则K 与K
与K 、K
、K 二者的关系为????????????????。
二者的关系为????????????????。
(3)已知某温度下,反应2SO +0
+0
 2S0
2S0 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积
固定的密闭容器中,co(SO )=lmol・L
)=lmol・L c0(O
c0(O )=1mol・L
)=1mol・L ,当反应在该温度下SO
,当反应在该温度下SO 转化率
转化率
为80%时,该反应????????(填“是”或“否”)达到化学平衡状态,若未达到,向 ????????
????????
(填“正反应”或“逆反应”)方向进行。
(4)对于可逆反应:aA(g)+bB(g)  cC(g)+riD(g)△H=
cC(g)+riD(g)△H= kJ・mol
kJ・mol ;若
;若 +b>
+b>
c+d,增大压强平衡向??????(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向
逆反应方向移动,则 ?????0(填“>”或“<”)。
?????0(填“>”或“<”)。