微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于硝酸性质的下列叙述中,不正确的是.
A.硝酸是无色、易挥发、有刺激性气味的液体
B.硝酸不稳定,浓度越大越易分解
C.硝酸与硫化钠反应能产生H2S气体
D.将铁粉与热的浓硝酸混合反应,产物中不一定有Fe(NO3)2
参考答案:C
本题解析:H2S具有强还原性,而HNO3具有强氧化性,两者会发生氧化还原反应.
本题难度:困难
2、选择题 下列说法不正确的是
A.σ键比π键重叠程度大,形成的共价键强
B.两个原子之间形成共价键时,最多有一个σ键
C.气体单质中,一定有σ键,可能有π键
D.N2分子中有一个σ键,2个π键
参考答案:C
本题解析:试题分析:σ键是头对头重贴形成的,π键是肩并肩重贴形成的,所以.σ键比π键重叠程度大,形成的共价键强,A正确;单键都是σ键,双键是由1个σ键,1个π键形成的。三键是由1个σ键,2个π键构成的,所以选项BD正确,C不正确,例如稀有气体分子中不存在化学键,答案选C。
考点:考查σ键、π键的有关判断和应用
点评:该题是高考中的常见考点,属于基础性试题的考查。试题紧扣教材,基础性强。主要是考查学生对σ键、π键的熟悉了解程度,以及灵活运用基础知识解决实际问题的能力的培养。
本题难度:简单
3、选择题 下列说法中正确的是
①金属氧化物不一定是碱性氧化物
②物质导电过程中必然要发生化学变化
③过氧化钠强有氧化性,也有还原性
④Fe(OH)3、FeCl2、Na2O2、H2SiO3都能直接用化合反应制备
⑤能跟碱反应的氧化物,一定是酸性氧化物
⑥苯酚和己烯使溴的水溶液褪色能用同一原理解释.
A.②③⑤
B.①③
C.①②③⑥
D.①②③⑤
参考答案:B
本题解析:分析:①金属氧化物不一定是碱性氧化物,如氧化铝;
②金属导电没有发生化学变化;
③过氧化钠中氧元素为-1价,强有氧化性,也有还原性;
④二氧化硅不能与水反应;
⑤能跟碱反应的氧化物,不一定是酸性氧化物,如氧化铝;
⑥苯酚与溴发生取代反应,己烯与溴发生加成反应.
解答:①碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物,如:氧化铝为两性氧化物,有些金属氧化物为酸性氧化物,故①正确;
②电解质或电解质溶液导电,一定发生化学变化,但金属导电没有发生化学变化,故②错误;
③过氧化钠中氧元素为-1价,强有氧化性,也有还原性,故③正确;
④氢氧化亚铁与氧气、水化合生成Fe(OH)3,铁与氯化铁化合生成FeCl2,钠与氧气化合生成Na2O2,但二氧化硅不能与水反应,不能通过化合反应导电硅酸,故④错误;
⑤能跟碱反应的氧化物,不一定是酸性氧化物,如氧化铝是两性氧化物,故⑤错误;
⑥苯酚与溴发生取代反应,己烯与溴发生加成反应,二者使溴水褪色原理不同,故⑥错误,
故选B.
点评:本题综合性较大,涉及化学基本概念、元素化合物性质、有机物性质等,难度不大,旨在考查学生对基础知识的理解掌握.
本题难度:简单
4、选择题 在同温同压下,关于等质量的CO2和SO2气体,下列说法不正确的是
A.CO2和SO2的分子数比为16:11
B.CO2和SO2的物质的量相同
C.CO2和SO2的体积比为16:11
D.CO2和SO2的密度比为11:16
参考答案:B
本题解析:分析:同温同压下,气体的Vm相等,根据n=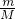 =
= =
=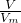 计算相关物理量.
计算相关物理量.
解答:A.N(CO2)=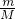 ×NA=
×NA=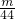 NA,N(SO2)=
NA,N(SO2)=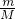 ×NA=
×NA=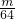 NA,二者的分子数比为64:44=16:11,故A正确;
NA,二者的分子数比为64:44=16:11,故A正确;
B.n(CO2)=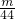 mol,n(SO2)=
mol,n(SO2)=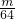 mol,二者的物质的量不同,故B错误;
mol,二者的物质的量不同,故B错误;
C.由n=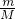 =
=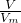 可知,同温同压下,等质量的两种气体的体积之比与摩尔质量呈反比,为64:44=16:11,故C正确;
可知,同温同压下,等质量的两种气体的体积之比与摩尔质量呈反比,为64:44=16:11,故C正确;
D.由ρ= =
=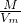 可知,二者的密度之比与摩尔质量呈正比,为44:64=11:16,故D正确.
可知,二者的密度之比与摩尔质量呈正比,为44:64=11:16,故D正确.
故选B.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,注意把握相关计算公式的推导及应用.
本题难度:一般
5、选择题 含有非极性键的离子化合物是
A.NH4Cl
B.NaOH
C.Na2O2
D.MgCl2
参考答案:C
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。含有离子键的化合物是离子化合物,全部由非极性键形成的化合物是共价化合物。所以A是含有离子键和极性键的离子化合物,B中是含有离子键和极性键的离子化合物,C是含有离子键和非极性键的离子化合物,D是含有离子键的离子化合物。因此答案选C。
本题难度:一般