微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某探究小组用洗净的废铜屑制备硝酸铜,下列方案中既节约原料又环保的是
A.Cu+HNO3(浓)→Cu(NO3)2
B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu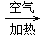 CuO
CuO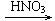 Cu(NO3)2
Cu(NO3)2
D.Cu  CuSO4
CuSO4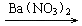 Cu(NO3)2
Cu(NO3)2
参考答案:C
本题解析:
试题分析:A.浓硝酸与铜反应生成污染性气体NO2,故A错误;
B.稀硝酸与铜反应生成污染性气体NO,故B错误;
C.铜与氧气反应生成CuO,与硝酸反应消耗硝酸最少,且没有生成污染性气体,故C正确;
D.铜与浓硫酸反应生成污染性气体二氧化硫,故D错误。
故选C。
点评:本题考查硝酸的性质,题目难度不大,本题注意常见元素化合物的性质,做题时注意从题目要求出发,把握原子经济问题。
本题难度:简单
2、实验题 (15分)某研究性学习小组设计实验探究铝等金属的性质:将铝片(不除氧化膜)投入浓氯化铜溶液中,铝表面很快出现一层海绵状暗红色物质,接下来铝片上产生大量气泡。触摸容器知溶液温度迅速上升,收集气体,检验其具有可燃性。若用同样的铝片投入同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。
⑴铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因可能是???????。
A.氯化铜溶液酸性比同浓度的硫酸铜溶液酸性强
B.硫酸铜水解生成硫酸使铝钝化
C.氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能
D.生成氯化铝溶于水,而生成硫酸铝不溶于水
请设计一个简单实验验证你的选择:??????????????????。
⑵铝片表面出现的暗红色物质的过程中发生的离子反应方程式是?????。用离子方程式解释产生气泡的原因:?????????。
⑶放出的气体是?????,请从有关物质的浓度、能量、是否有电化学作用等分析开始阶段产生气体的速率不断加快的原因是????????????????????????????????????????。(写出一点即可)
⑷某同学通过一定的实验操作,也能使铝片与硫酸铜溶液反应加快,他采取的措施可能是??????????。
A.用砂纸擦去铝片表面的氧化膜后投入硫酸铜溶液中
B.把铝片投入热氢氧化钠溶液中一段时间后,取出洗涤,再投入硫酸铜溶液中
C.向硫酸铜溶液中滴加氢氧化钠溶液,再投入铝片
D.在铝片上捆上几枚铜钉后投入同浓度的硫酸铜溶液中
⑸除去氧化铝的铝片与铜片为电极,在X电解质溶液中构成原电池,列表如下:
选项
| 铝电极
| 电解质
| 负极反应
| 正极反应
|
A
| 正极
| NaOH
| Al-3e-=Al3+
| 2H2O+2e-=2OH-+H2↑
|
B
| 负极
| 稀盐酸
| 2Al-6e-=2Al3+
| 6H++6e-=3H2↑
|
C
| 正极
| 浓硝酸
| Cu-2e--=Cu2+
| 2NO3-+4H+-4e-=2NO2↑+2H2O
|
D
| 负极
| 稀硝酸
| Cu-2e-=Cu2+
| 2NO3-+8H+=2NO↑+4H2O+6e-
其中正确的是????,由此推知,金属作电极不仅与本身性质相关,而且与 ________?有关。
参考答案:(15分)⑴C (1分)在硫酸铜溶液中加入铝片,无明显现象,
本题解析:略
本题难度:一般
3、实验题 亚铁是血红蛋白重要组成成分,起着向人体组织传送O2的作用,如果缺铁就可能出现缺铁性贫血,但是摄入过量的铁也有害。下面是一种常见补药品说明书中的部分内容:该药品含Fe2+33%~36%,不溶于水但能溶于人体中的胃酸:与Vc(维生素C)同服可增加本品吸收。
(一)甲同学设计了以下下实验检测该补铁药品中是否含有Fe2+并探究Vc的作用:
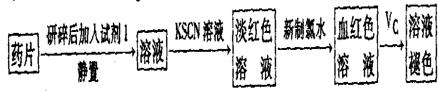
(1)加入新制氯水后溶液中发生的离子反应方程式是_________、
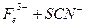 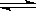 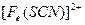 。 。
(2)加入KSCN溶液后溶液变为淡红色,说明溶液中有少量Fe3+。该离子存在的原因可能是(填编号)_____________________。
A.药品中的铁本来就应该以三价铁的形式存在
B.在制药过程中生成少量三价铁
C.药品储存过程中有少量三价铁生成
(3)向血红色溶液中加入一片Vc片,片刻后溶液血红色褪去,说明Vc有_______性;药品说明书中”与Vc同服可增加本品吸收”请说明理由_______________________。
(二)乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为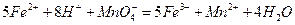 。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。 。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(4)该实验中的试剂2与甲同学设计的实验中的试剂1都可以是______(填序号)。
A.蒸馏水?????? B.稀盐酸?????? C.稀硫酸?????? D.稀硝酸
(5)本实验滴定过程中操作滴定管的图示正确的是_______(填编号)。
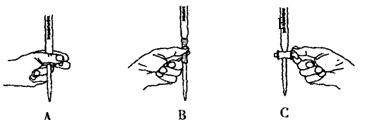
(6)请通过计算,说明该药品含“铁”量是否合格(写出主要计算过程)?
参考答案:(1) 本题解析:略 本题解析:略
本题难度:简单
4、选择题 通过观察法不能确定下列物质是否变质的是( )
A.FeSO4
B.Na2O2
C.C6H5OH
D.Na2SO3
参考答案:D
本题解析:
本题难度:一般
5、实验题 某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
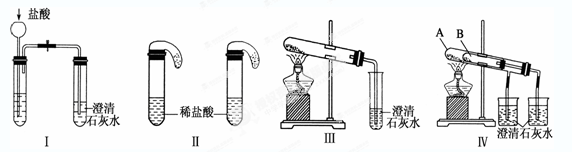
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)___???_______;
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其都发生的反应的化学方程式为_____________???????????????????___________;与实验Ⅲ相比,实验Ⅳ的优点是__________________________;
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是________;
(4)有同学认为,除上述试验方法外,向两种固体配成的溶液中加入澄清石灰水也可以区分它们,这种说法是_____________(填“正确”或“错误”)的。
(5)将碳酸氢钠溶液与足量的澄清石灰水混合并充分反应,其离子方程式为_________________________。其剩余溶液的溶质化学式为___________
(6)另有两瓶溶液,已知分别是K2CO3和NaHCO3,请你写出两种不同的鉴别方法。
①________________________________________________________________________;
②_______________________________________________________________________。
参考答案:(1)Ⅱ(2)2NaHCO3 本题解析: 本题解析:
试题分析:(1)无论碳酸钠还是碳酸氢钠都能和盐酸反应生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,故Ⅰ无法鉴别;实验Ⅱ中,盐酸和碳酸氢钠反应立即产生气泡,盐酸和碳酸钠先反应生成碳酸氢钠,碳酸氢钠和盐酸反应生成二氧化碳气体,所以看到的现象不同,故能鉴别碳酸钠和碳酸氢钠。
(2)碳酸氢钠在加热条件下能分解生成碳酸钠、水和二氧化碳,反应的化学方程式是2NaHCO3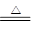 Na2CO3+H2O+CO2↑。CO2能使澄清的石灰水变混浊,则反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O。与实验相比,实验Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行。 Na2CO3+H2O+CO2↑。CO2能使澄清的石灰水变混浊,则反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O。与实验相比,实验Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行。
(3)碳酸钠直接加热,碳酸氢钠不直接加热,不直接加热的碳酸氢钠能分解而直接加热的碳酸钠不分解更能说明碳酸氢钠不稳定,所以试管B中装入的固体最好是碳酸氢钠。
(4)澄清石灰水均能和碳酸氢钠以及碳酸钠反应生成白色沉淀碳酸钙,不能鉴别,所以这种说法是错误的。
(5)如果澄清的石灰水过量,则碳酸氢钠和石灰水反应生成物是碳酸钙、氢氧化钠和水,反应的离子方程式是HCO3-+Ca2++OH-=CaCO3↓+H2O。因此剩余溶液的溶质化学式为Ca(OH)2、NaOH。
(6)①根据盐中阳离子的不同,可以通过焰色反应鉴别,即利用焰色反应,隔蓝色钴玻璃观察,能看到紫色焰色的是K2CO3,否则是2NaHCO3。
②根据盐中阴离子的不同,可以利用沉淀法鉴别。即加入BaCl2(CaCl2)溶液,产生白色沉淀的是K2CO3,否则是2NaHCO3。
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。明确物质的性质和实验原理,是答题的关键。
本题难度:一般
|