微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (13分)某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】用葡萄糖制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag。
【设计实验方案,验证假设】
(1)甲同学从上述实验的生成物中检验出Fe2+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:????????????????????????。甲同学还发现用同浓度FeCl3,Fe(NO3)3溶解银镜,FeC l3溶液溶解Ag的反应更快更完全,请解释其原因:
l3溶液溶解Ag的反应更快更完全,请解释其原因:
(2)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
实验步骤(不要求写具体操作过程)
| 预期现象和结论
|
①
②
……
| 若银镜消失,假设2成立。
若银镜不消失,假设2不成立。
【思考与交流】
(3)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO3-都氧化了Ag。
你是否同意丙同学的结论??????,并简述理由:????????????????????????????。
参考答案:(1)Fe3++Ag= Fe2++Ag+(2分)?? FeC
本题解析:略
本题难度:简单
2、选择题 用如图所示的方法研究某气体的性质,这种方法属于
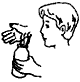 [???? ] [???? ]
A.分类法
B.观察法
C.实验法
D.比较法
参考答案:B
本题解析:
本题难度:简单
3、实验题 某同学用标准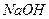 溶液来测定未知浓度的盐酸的浓度: 溶液来测定未知浓度的盐酸的浓度:
(1)配制250mL 0.5mol/L的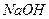 溶液所需的玻璃仪器为????????????????????????。 溶液所需的玻璃仪器为????????????????????????。
(2)用滴定管准确量取20.00mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用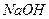 溶液滴定到终点。 溶液滴定到终点。
该同学进行了三次实验,实验数据如下表:
实验编号
| 盐酸的体积(mL)
| 标准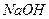 溶液的体积(mL) 溶液的体积(mL)
| 1
| 20.00
| 18.20
| 2
| 17.10
| 3
| 16.90
?
滴定中误差较大的是第??????次实验,造成这种误差的可能原因是??????(填选项编号)
a、在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
b、滴定管在盛装标准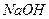 溶液前未润洗 溶液前未润洗
c、滴定开始前盛装标准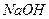 溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡 溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
d、滴定开始前盛装标准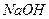 溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡 溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f、达到滴定终点时,俯视溶液凹液面最低点读数
g、滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸的物质的量浓度为??????????????????????(结果保留三位小数)。
参考答案:(1)烧杯、玻璃棒、250mL容量瓶、胶头滴管。(4分)
本题解析:略
本题难度:简单
4、实验题 某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
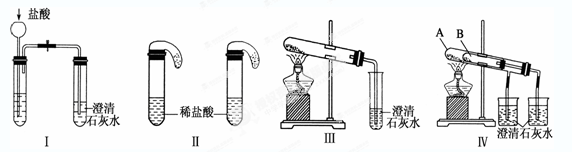
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)___???_______;
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其都发生的反应的化学方程式为_____________???????????????????___________;与实验Ⅲ相比,实验Ⅳ的优点是__________________________;
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是________;
(4)有同学认为,除上述试验方法外,向两种固体配成的溶液中加入澄清石灰水也可以区分它们,这种说法是_____________(填“正确”或“错误”)的。
(5)将碳酸氢钠溶液与足量的澄清石灰水混合并充分反应,其离子方程式为_________________________。其剩余溶液的溶质化学式为___________
(6)另有两瓶溶液,已知分别是K2CO3和NaHCO3,请你写出两种不同的鉴别方法。
①________________________________________________________________________;
②_______________________________________________________________________。
参考答案:(1)Ⅱ(2)2NaHCO3 本题解析: 本题解析:
试题分析:(1)无论碳酸钠还是碳酸氢钠都能和盐酸反应生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,故Ⅰ无法鉴别;实验Ⅱ中,盐酸和碳酸氢钠反应立即产生气泡,盐酸和碳酸钠先反应生成碳酸氢钠,碳酸氢钠和盐酸反应生成二氧化碳气体,所以看到的现象不同,故能鉴别碳酸钠和碳酸氢钠。
(2)碳酸氢钠在加热条件下能分解生成碳酸钠、水和二氧化碳,反应的化学方程式是2NaHCO3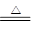 Na2CO3+H2O+CO2↑。CO2能使澄清的石灰水变混浊,则反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O。与实验相比,实验Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行。 Na2CO3+H2O+CO2↑。CO2能使澄清的石灰水变混浊,则反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O。与实验相比,实验Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行。
(3)碳酸钠直接加热,碳酸氢钠不直接加热,不直接加热的碳酸氢钠能分解而直接加热的碳酸钠不分解更能说明碳酸氢钠不稳定,所以试管B中装入的固体最好是碳酸氢钠。
(4)澄清石灰水均能和碳酸氢钠以及碳酸钠反应生成白色沉淀碳酸钙,不能鉴别,所以这种说法是错误的。
(5)如果澄清的石灰水过量,则碳酸氢钠和石灰水反应生成物是碳酸钙、氢氧化钠和水,反应的离子方程式是HCO3-+Ca2++OH-=CaCO3↓+H2O。因此剩余溶液的溶质化学式为Ca(OH)2、NaOH。
(6)①根据盐中阳离子的不同,可以通过焰色反应鉴别,即利用焰色反应,隔蓝色钴玻璃观察,能看到紫色焰色的是K2CO3,否则是2NaHCO3。
②根据盐中阴离子的不同,可以利用沉淀法鉴别。即加入BaCl2(CaCl2)溶液,产生白色沉淀的是K2CO3,否则是2NaHCO3。
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。明确物质的性质和实验原理,是答题的关键。
本题难度:一般
5、实验题 化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。某研究性学习小组用如下图装置进行铜与浓硫酸反应的实验研究。
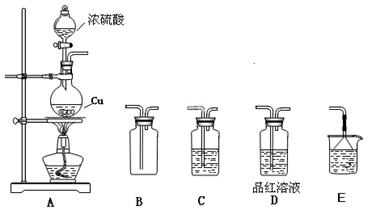
(1)装置A中发生反应的化学方程式???????????????????????????;
(2)若要使B 中收集满干燥的SO2气体(并证实B中已收集满),则上述装置的连接顺序为:???接???接????接??接???(用字母表示);
(3)C 中盛放的试剂是??????????,证明B 中已收集满SO2的现象是?????????????;
(4)待烧瓶中充分反应后,同学们发现铜有剩余,经检测发现硫酸也有剩余。检验硫酸有剩余的方法是???????????___________________;
(5)在不补充浓硫酸的前提下,为使铜进一步溶解,可向烧瓶中加入????????? ________(填序号)。① 盐酸 ?② FeSO4?? ③ Fe2O3??? ④KNO3
参考答案:(1)Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2
本题解析:略
本题难度:一般
|
|