微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是(??)
A.溶液中导电粒子的数目减少
B.溶液中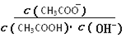 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH<7
参考答案:B
本题解析:
试题分析:A、醋酸是弱电解质,加水稀释,电离平衡正向移动,导致溶液中导电粒子的数目增多,错误;B、温度不变,所以电离平衡常数不变,正确;C、加水稀释,电离平衡正向移动,醋酸的电离程度增大,但氢离子增加的数目不及溶液体积增加的幅度大,所以c(H+)减小,错误;D、若醋酸不稀释,加入10 mL pH=11的NaOH溶液,混合液pH<7,稀释后的溶液的pH不能确定,因为未指明稀释的倍数,错误,答案选B。
本题难度:一般
2、选择题 下列事实一定能说明HNO2为弱电解质的是
①常温下Na NO2溶液的PH>7 ②10mL1mol/L HNO2恰好与10mL1mol/LNaOH完全反应③HNO2与NaCl不能反应④0.1mol/L HNO2溶液的PH=2.1
A:①②③④ B:②③④ C:①④ D:②④
参考答案:C
本题解析:略
本题难度:一般
3、选择题 下列事实可证明氨水是弱碱溶液的是(??? )。
A.氨水能被弱酸醋酸中和
B.铵盐受热易分解
C.氨水可以使酚酞试液变红
D.0.lmol/L氯化铵溶液的pH约为5
参考答案:D
本题解析:
试题分析:A、只能说明氨水是碱溶液,错误;B、铵盐受热易分解说明铵盐对热不稳定,错误;C、氨水可以使酚酞试液变红,说明氨水显碱性,错误;D、0.lmol/L氯化铵溶液的pH约为5,溶液显酸性,说明铵根离子水解生成了弱碱NH3・H2O,使溶液中的c(H+)>c(OH-),正确,答案选D。
本题难度:简单
4、填空题 (11分)在t℃时,某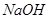 稀溶液中,
稀溶液中, ,
, ,已知
,已知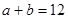 ,则:
,则:
(1)该温度下,水的离子积常数Kw=__________________。
(2)在该温度下,将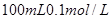 的稀硫酸与
的稀硫酸与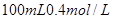 的
的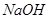 溶液混合后,溶液的pH=_________,此时该溶液中由水电离的
溶液混合后,溶液的pH=_________,此时该溶液中由水电离的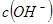 =_________。
=_________。
(3)该温度下,若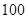 体积
体积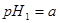 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的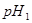 与强碱的
与强碱的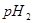 之间应满足的关系是_________。
之间应满足的关系是_________。
(4)该温度下, 的硫酸溶液和
的硫酸溶液和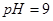 的
的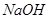 溶液等体积混合后,混合溶液的
溶液等体积混合后,混合溶液的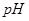 _________(填>7、=7、<7);
_________(填>7、=7、<7); 的醋酸溶液和
的醋酸溶液和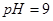 的
的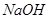 溶液等体积混合后,混合溶液的
溶液等体积混合后,混合溶液的 _________(填>7、=7、<7)。
_________(填>7、=7、<7)。
参考答案:(11分,第一个空1分,其它每空2分)(1)![]()
本题解析:(1)Kw=c(H+)c(OH-)=10-a×10-b=10-(a+b)=10-12(2)首先酸碱中和,NaOH过量,c(OH-)==0.1mol/L,pH=-lg=11,水电离的氢氧根为10-11mol/L,(3)n(H+)=n(OH-),100×10-a=1×10-(12-b),a+b=14;(4)pH=3和pH=9的酸碱,氢离子和氢氧根离子浓度相等,中和后pH=6,醋酸和氢氧化钠中和,醋酸过量呈酸性,pH<6。
本题难度:一般
5、简答题 下列物质①Cu②液态SO2③纯醋酸④NaHCO3⑤Ba(OH)2溶液
I、属于非电解质的是______;(填序号)
Ⅱ、(1)NaHCO3是一种______(填“强”或“弱”)电解质;
(2)写出HCO3-水解的离子方程式:______;
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH-五种微粒的浓度由大到小的顺序为:______.
(4)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5mol?L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3?HCO3-+H+的平衡常数K1=______.(已知:10-5.60=2.5×10-6)
Ⅲ、Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)该Ba(OH)2溶液的物质的量浓度为______;
(2)溶液中由水电离出c(OH-)=______;
(3)与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=______.
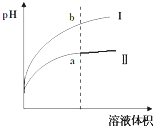
Ⅳ、醋酸是一种弱电解质.某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如右图所示.则图______(填“I”或“Ⅱ”)为醋酸稀释的图象.
参考答案:Ⅰ、①Cu是金属单质能导电,但单质即不是电解质也不是非电解质
本题解析:
本题难度:简单