微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)Ⅰ 现欲用碳酸钙固体和稀盐酸反应制取CO2气体,请回答下列问题:
⑴写出发生反应的离子方程式________________________________;
⑵实验过程中绘制出生成CO2的体积[V(CO2)]与时间(t)的关系如图所示,试分析判断OE段、EF段、FG段反应速率(分别用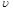 (OE)、
(OE)、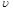 (EF)、
(EF)、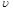 (FG)表示)哪个最快______________;
(FG)表示)哪个最快______________;
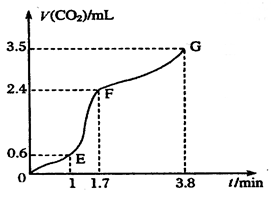
比较OE段和EF段,说明EF段速率变化的主要原因可能是______________????? ____
Ⅱ 反应A + 3B =" 2C" + 2D。在四种不同的情况下的反应速率分别为:
①υ(A)=0.15mol/(L・s)???? ②υ(B)=0.6mol/(L・s)
③υ(C)=0.4mol/(L・s)????? ④υ(D)=0.45mol/(L・s)
该反应进行的快慢顺序为__???????????。
参考答案:(8分)
Ⅰ⑴CaCO3+2H+=Ca2++H2O+C
本题解析:I:反应速率是指单位时间内物质的量的改变值,在图像是当然是斜率大的地方速率大;速率主要决定于反应物的本性,但也受外界如温度、浓度等的影响。本反应开始后EF段的速率却最大,说明反应物浓度较大,但最主要的还是反应放出的热量所致。
II:把四个速率以方程式系数比为标准转化为同一物质的速率再进行比较。
本题难度:一般
2、选择题 900 ℃时,向2.0 L恒容密闭容器中充入0.40 mol乙苯,发生反应:
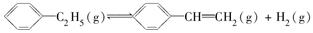 ΔH=a kJ・mol-1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
ΔH=a kJ・mol-1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
时间/min
| 0
| 10
| 20
| 30
| 40
|
n(乙苯)/mol
| 0.40
| 0.30
| 0.24
| n2
| n3
|
n(苯乙烯)/mol
| 0.00
| 0.10
| n1
| 0.20
| 0.20
?
下列说法正确的是( )。
A.反应在前20 min的平均速率为v(H2)=0.008 mol・L-1・min-1
B.保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08 mol・L-1,则a<0
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0%
D.相同温度下,起始时向容器中充入0.10 mol乙苯、0.10 mol苯乙烯和0.30 mol H2,达到平衡前v正>v逆
参考答案:C
本题解析:根据题意

起始:0.40 mol ??? 0 mol 0 mol
变化:0.16 mol ??? 0.16 mol ??? 0.16 mol
20 min:0.24 mol ???? 0.16 mol ? 0.16 mol
则反应在前20 min的
本题难度:一般
3、计算题 在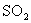 、 、 转化为 转化为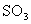 的反应中, 的反应中,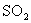 的起始浓度为 的起始浓度为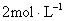 , , 的起始浓度为 的起始浓度为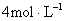 ,3min后 ,3min后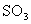 的浓度为 的浓度为 。计算该反应的反应速率是多少?3min 时的 。计算该反应的反应速率是多少?3min 时的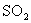 和 和 的浓度各是多少? 的浓度各是多少?
参考答案:详见解析
本题解析:计算化学反应速率的关键在于依据给出条件,正确求出各物质转化浓度,用转化浓度除以反应时间,就可以得到反应速率,转化浓度求法简单,对于反应物来说:
转化浓度 = 起始浓度-终了浓度
对于生成物来说:
转化浓度 = 终了浓度-起始浓度
本题给出生成物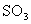 的终了浓度为 的终了浓度为![]()
本题难度:简单
4、选择题 我们主要从三个方面讨论一个化学反应的原理,其中不属于这三个方面的是 [???? ]
A.反应进行的方向
B.反应的快慢
C.反应进行的限度
D.反应物的多少
参考答案:D
本题解析:
本题难度:简单
5、选择题 下图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )

A.A是反应物
B.前2 min A的分解速率为0.1 mol・L-1・min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.反应的方程式为:2A(g) 2B(g)+C(g) 2B(g)+C(g)
参考答案:C
本题解析:据题意知A为反应物,B、C为生成物,Δn(A)∶Δn(B)∶Δn(C)=(0.4 mol・L-1-0.2 mol・L-1)∶(0.3 mol・L-1-0.1 mol・L-1)∶0.1 mol・L-1=2∶2∶1,故反应方程式为2A(g) 2B(g)+C(g);前2 min A的分解速率为 2B(g)+C(g);前2 min A的分解速率为 本题难度:简单 本题难度:简单
|