微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 钢铁发生吸氧腐蚀时,正极上发生的反应是
A.2Fe-4e― =2Fe2+
B.2Fe2++4e― =2Fe
C.2H2O+O2+4e―=4OH―
D.Fe3++e―=Fe2+
参考答案:C
本题解析:略
本题难度:一般
2、选择题 已知电池总反应为:Zn+2MnO2+H2O ZnO+2MnO(OH)。下列说法正确的是
ZnO+2MnO(OH)。下列说法正确的是
A.放电时,Zn为负极,ZnO为正极,MnO2为催化剂
B.放电时,该电池的正极反应为:MnO2+e-+H2O=MnO(OH)+OH-
C.充电时,电池将化学能转为电能
D.放电时,溶液中的阴离子向原电池的正极移动
参考答案:B
本题解析:
试题分析:放电时,Zn为负极,MnO2为正极,A错误;放电时正极发生还原反应,B正确;充电时电能转变为化学能,C错误;放电时阴离子向负极移动,D错误。答案选B。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断。
本题难度:一般
3、选择题 如图,缠上金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到在金属条表面的溶液出现粉红色。该金属条可能是??? ( )。
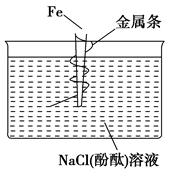
A.铜
B.镁
C.铝
D.锌
参考答案:A
本题解析:出现粉红色说明金属条附近产生了OH-,发生了吸氧腐蚀,金属条作正极,其活泼性比铁要差。
本题难度:简单
4、选择题 下列叙述不正确的是
A.白铁(镀锌铁)镀层破损后,先被腐蚀的是铁
B.锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
C.钢铁表面常易锈蚀生成Fe?2O3・nH2O
D.金属的腐蚀主要是电化学腐蚀
参考答案:A
本题解析:试题分析:锌的金属性强于铁的,所以白铁(镀锌铁)镀层破损后,先被腐蚀的是锌,铁被保护,A不正确,其余选项都是正确的,答案选A。
考点:考查电化学的综合应用
点评:金属失去电子而被氧化的过程是金属的腐蚀,金属腐蚀主要是以电化学腐蚀为主。而金属的防护也主要是借助于电化学原理进行,主要是牺牲阳极的阴极保护法和外接电源的阴极保护法,据此可以进行有关判断。
本题难度:一般
5、填空题 (每空2分,共12分)
(Ⅰ)钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀。在空气酸度不大的环境中,其负极是??????,负极反应式为???????????????????????;正极是??????,正极反应式为?????????????????????????????????。受空气的影响还会发生相应的颜色变化,其相应的化学方程式为????????????????????????。
(Ⅱ)下列各情况,在其中Fe片腐蚀由快到慢的顺序是(用序号表示)?????????????????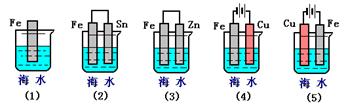
参考答案:(每空2分,共12分)(Ⅰ)铁???????? Fe-2 e
本题解析:(1)考查钢铁的电化学腐蚀。钢铁发生电化学腐蚀时,铁是负极,失去电子,电极反应式是Fe-2 e- = Fe2+;如果在空气酸度不大的环境中,发生的是吸氧腐蚀,正极反应式是O2 +4 e- + 2H2O =" 4" OH- ;生成的亚铁离子和OH-离子结合生成氢氧化亚铁,氢氧化亚铁不稳定,极易被氧气氧化生成红褐色氢氧化铁,反应的方程式是
4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(Ⅱ)装置(1)是铁的化学腐蚀。装置(2)、(3)中都是原电池,由于金属性强弱顺序是锌、铁、锡,所以在装置
本题难度:一般