微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在溶液中加入足量Na2O2后仍能大量共存的离子组是
A.NH4+、Ba2+、 Cl-、 NO3-
B.K+、 AlO2-、Cl-、SO42-
C.Ca2+、Na+、NO3-、 HCO3-
D.Na+、Cu2+ 、Cl-、NO3-
参考答案:B
本题解析:试题分析:Na2O2既有氧化性,又有碱性,因此有还原性的离子和不能与OH-共存的离子都不能大量存在。A中的NH4+,C中的HCO3-,D中的Cu2+。答案选B。
考点:离子共存
点评:离子不能大量共存的一般情况是:(1)能发生复分解反应的离子之间(即生成沉淀,气体,水、弱酸、弱碱等难电离物质);(2)能生成难溶物的离子之间(如:Ca2+和 SO42-;Ag+和 SO42-);(3)能完全水解的离子之间,如多元弱酸和弱碱盐的阴、阳离子(如:Al3+, Fe3+与 CO32-、HCO3-、AlO2-、ClO-,S2-等);(4)能发生氧化还原反应的离子之间(如:Fe 、H+、NO3-;S2-、ClO-;S2-、 Fe3+等);(5)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。
本题难度:困难
2、选择题 已知SO32-+I2+H2O=SO42-+2I-+2H+。某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色。则下列关于该溶液组成的判断正确的是[???? ]
A.肯定不含I-
B.肯定不含Cu2+
C.可能含有SO32-
D.肯定不含有NH4+
参考答案:B
本题解析:
本题难度:简单
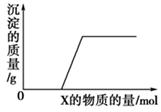
3、选择题 将溶液(或气体)X逐渐加入(或通入)到一定量的Y溶液中,产生沉淀的质量与加入X的物质的量关系如图所示,符合图中情况的一组物质是( )
?
| X
| Y溶液
|
A
| Ba(HCO3)2溶液
| NaOH溶液
|
B
| KOH溶液
| Mg(HSO4)2溶液
|
C
| Na2CO3溶液
| CaCl2溶液
|
D
| CO2气体
| 石灰水
?
参考答案:B
本题解析:选项A中立即生成碳酸钡沉淀,不正确;选项B中,氢氧化钾首先中和溶液中的氢离子,然后再生成氢氧化镁沉淀,因此B正确;选项C中也是立即生成碳酸钙沉淀,不正确;选项D中先生成碳酸钙沉淀,当沉淀不再发生变化时,继续通入CO2,沉淀开始溶解生成碳酸氢钙,D不正确,所以正确的答案选B。
本题难度:一般
4、选择题 下列离子组一定能大量共存的是
A.滴加甲基橙后呈黄色的溶液中:I-、Cl-、ClO-、Na+
B.pH=13的溶液中:Na+、CO32-、NO3-、HCO3-
C.含大量OH一的溶液中:CO32-、Cl-、F-、K+
D.含大量Al3+的溶液中:K+、Na+、NO3-、AlO2-
参考答案:C
本题解析:分 析:A.滴加甲基橙后呈黄色的溶液,显酸性或碱性;
B.pH=13的溶液,显碱性;
C.该组离子之间不反应;
D.离子之间相互促进水解.
解答:A.滴加甲基橙后呈黄色的溶液,显酸性或碱性,氢离子与I-、ClO-发生氧化还原反应,则不能共存,故A错误;
B.pH=13的溶液,显碱性,OH-与HCO3-反应生成水和碳酸根离子,则不能共存,故B错误;
C.该组离子之间不反应,则能共存,故C正确;
D.Al3+、AlO2-离子之间相互促进水解生成沉淀,则不能共存,故D错误;
故选C.
点评:本题考查离子的共存,明确习题中的信息及离子之间的反应是解答本题的关键,注意发生的氧化还原反应和相互促进水解的反应,题目难度不大.
本题难度:简单
5、选择题 下列关于实验或说法正确的是(???)
A.SO2能使品红溶液、酸性KMnO4溶液褪色,加热后都能复原
B.用铂丝蘸取某溶液在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰颜色为紫色,说明原溶液中不含Na+
C.用滴加BaCl2溶液,观察有无白色沉淀的方法来鉴别K2CO3和NaHCO3
D.少量CO2通过CaCl2的溶液能生成白色沉淀,过量CO2时白色沉淀溶解
参考答案:C
本题解析:A项,因二者漂白原理不同,SO2能使品红溶液褪色后加热能复原,酸性KMnO4溶液褪色后不复原;B项,也可能含有Na+,因为即使有钠离子也可能被蓝色钴玻璃滤去了;D项,无论少量还是过量,都无白色沉淀生成。
本题难度:一般
|