��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��100��ʱ����0.100mol��N2O4�������1L��յ��ܱ������У���һ��ʱ��Ը������ڵ����ʽ��з������õ������
ʱ��/s
Ũ��mol?L-1 | 0 | 20 | 40 | 60 | 80 | 100
c��N2O4��mol?L-1
0.100
c1
0.050
c3
a
b
c��NO2��/mol?L-1
0.000
0.060
c2
0.120
0.120
0.120
����գ�
��1���ﵽƽ��ʱN2O4��ת����Ϊ______%������c2______c3��a______b?��ѡ�������������=������
��2��20s��������������Ũ��c1=______mol?L-1����0s��20s��������������ƽ����Ӧ����Ϊ______mol?��L?s��-1����
��3��������ͬ���������������������Ƕ�����������Ҫ�ﵽ����ͬ����ƽ��״̬��������������ʼŨ����______mol?L-1��
2��ѡ���� ��һ���¶��£���a L�ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X��g����2Y��g��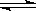 2Z��g�����˷�Ӧ�ﵽƽ��ı�־��?? 2Z��g�����˷�Ӧ�ﵽƽ��ı�־��??
A��������ѹǿ����ʱ��仯 | B���������ܶȲ���ʱ��仯
C��������X��Y��Z��Ũ��֮��Ϊ1�U2�U2
D����λʱ������0.1 mol Xͬʱ����0.2 mol Z
3��ѡ���� Ӱ�컯ѧ��Ӧ���ʵ�����Ҫ������
A.��Ӧ��Ľṹ������
B.����
C.��Ӧ���Ũ��
D.��Ӧ�¶�
4��ѡ���� ʹ2 mol N2��6 mol H2��Ϸ������з�Ӧ��N2(g)+3H2(g) 2NH3(g)������ӦΪ���ȷ�Ӧ��������˵��������� 2NH3(g)������ӦΪ���ȷ�Ӧ��������˵���������
A������ƽ����ϵ���¶ȣ�����������䣩����������ƽ����Է����������
B������ƽ����ϵ���¶ȣ�����������䣩�����������ܶȲ���
C������Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ���1��3
D�����ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫�����ƶ�
5��ѡ���� ��֪2SO2+O2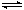 2SO3;��H��-92.6 kJ��mol-1������Ӧ�ﵽƽ��ʱ�����д�ʩ���ٽ����¶ȣ��ڼ�Сѹǿ������V2O5��������������O2��Ũ�ȣ�������SO2��Ũ�ȣ���ѹͨ��He���������SO2ת���ʵ��� 2SO3;��H��-92.6 kJ��mol-1������Ӧ�ﵽƽ��ʱ�����д�ʩ���ٽ����¶ȣ��ڼ�Сѹǿ������V2O5��������������O2��Ũ�ȣ�������SO2��Ũ�ȣ���ѹͨ��He���������SO2ת���ʵ���
A���٢ڢ�
B���٢ܢ�
C���ܢݢ�
D���٢�
|