微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知NO2和N2O4可以相互转化:2NO2(g) 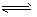 N2O4(g);△H<0。现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法错误的是
N2O4(g);△H<0。现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法错误的是
 [???? ]
[???? ]
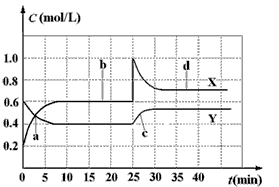
A.图中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C.反应进行至25 min时,曲线发生变化的原因是加入0.4 mol N2O4
D.若要达到与d相同的状态,在25 min时还能采取的措施是适当缩小容器体积
2、填空题 能源的相互转化和利用是科学家研究的重要课题.
(1)将水蒸气通过红热的炭即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ?mol-1,
①该反应能否自发进行的外界条件是______;
②在一个恒容的密闭容器中,一定温度下发生上述反应,下列能判断该反应达到化学平衡状态的是______(填相应的编号).
A.c(CO)=c(H2) B.1molH-H键断裂的同时断裂2mol H-O键
C.容器中的压强不变 D.消耗H2O的速率等于生成H2的速率
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,在催化剂存在下进行反应:CO(g)+H2O(g)?H2(g)+CO2(g),得到如下二组数据: