��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� X��Y��Z��W�Ƕ������г���Ԫ�أ��������Ϣ���±���
Ԫ��
| �����Ϣ
|
X
| XԪ���γɵ�һ��ͬ������������Ȼ������Ӳ�����ĵ���
|
Y
| ���³�ѹ�£�Y�����ǵ���ɫ���壬��������ڻ�ҩ
|
Z
| Z�Ļ�̬ԭ�Ӻ�����3���ܼ����е��ӣ�����3��������
|
W
| WԪ���γɵ�˫ԭ�ӷ��ӣ�������Ϊ���� ɫ���壬һ�ֳ�����ҵԭ��
��1��WԪ��λ��Ԫ�����ڱ��е� ���� �壬��Yͬ������λ�ڵ�������Ԫ�صĻ�̬ԭ�Ӻ�������Ų�ʽΪ ��
��2��XY2�����к��еĦҼ��ͦм�������Ϊ ������ͬ������XY2��XO2��ȣ��۵�ϸߵ��� (�ѧʽ)�����������۽���Z�������Ԫ�ص�һ�����ܴ���ͬ���ں�һ��Ԫ�ص�ԭ�� ��
��3��Y��WԪ���γɵĻ�����Y2W2�����⻯��ZH3����ˮ�����·�Ӧ����Y4Z4������Y8��һ�ֿ�����Ϊ���ʵ����ʣ���д����Ӧ��ѧ����ʽ�� ��
��4����֪����lmolY(s)ת��Ϊ��̬Y(g) ��������280 kJ��
��2XO(g)+O2(g)= 2XO2(g) ��H=-566.0KJ/mol��
��Y(s)+O2(g)=YO2(g) ��H=-299.0KJ/mol��һ�������£���������X��������XO��Y��������YO2����Y(g)���ʺ�X����������ﵽ������ȾĿ�ġ���д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
2��ѡ���� ��֪���з�Ӧ���Ȼ�ѧ����ʽ��
6C(s)��5H2(g)��3N2(g)��9O2(g)=2C3H5(ONO2)3(l) ��H1
2H2(g)��O2(g)=2H2O(g) ��H2
C(s)��O2(g)=CO2(g) ��H3
��Ӧ4C3H5(ONO2)3(l)=12CO2(g)��10H2O(g)��O2(g)��6N2(g)�Ħ�HΪ(����)��
A��12��H3��5��H2��2��H1
B��2��H1��5��H2��12��H3
C��12��H3��5��H2��2��H1
D����H1��5��H2��12��H3
3������� ��֪�Ȼ�ѧ����ʽ��
4Al��s��+3O2��g���T2Al2O3��s����H1=-3288.6kJ?mol-1��
4Fe��s��+3O2��g���T2Fe2O3��s����H2=-1631.8kJ?mol-1��
���������������������ȷ�Ӧ���Ȼ�ѧ����ʽΪ______��
4������� ��˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3(s)��3CO(g)��2Fe(s)��3CO2(g) ��H��-24��8kJ��mol
3Fe2O3(s)��CO(g)��2Fe3O4(s)��CO2(g) ��H��-47��2kJ��mol
Fe3O4(s)��CO(g)��3FeO(s)��CO2(g) ��H��+640��5kJ��mol
д��CO���廹ԭFeO����õ�Fe�����CO2������Ȼ�ѧ��Ӧ����ʽ��
___________________________
5������� ȼú�����еĵ������NOx����������̼�����壬�������з�����������ʵ�ֽ��ܼ��š��������õȡ�
��1����ȼú����������������ʱ�������ü������ԭ��������磺
CH4(g)��4NO2(g)��4NO(g)��CO2(g)��2H2O(g) ��H����574 kJ��mol��1
CH4(g)��4NO(g)��2N2(g)��CO2(g)��2H2O(g) ��H����1160 kJ��mol��1
��CH4(g)��NO2(g)��ԭΪN2(g)�ȵ��Ȼ�ѧ����ʽΪ ��
��2����ȼú�����е�CO2ת��Ϊ���ѵķ�Ӧԭ��Ϊ��
2CO2(g) + 6H2(g) 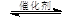 CH3OCH3(g) + 3H2O(g) CH3OCH3(g) + 3H2O(g)
��֪һ��ѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ת���ʼ��±���
Ͷ�ϱ�[n(H2) / n(CO2)]
| 500 K
| 600 K
| 700 K
| 800 K
| 1.5
| 45%
| 33%
| 20%
| 12%
| 2.0
| 60%
| 43%
| 28%
| 15%
| 3.0
| 83%
| 62%
| 37%
| 22%
�����¶����ߣ���Ӧ��ƽ�ⳣ��K�� �����������С�����䡱����ͬ�������¶Ȳ��䣬���Ͷ�ϱ�[n(H2) / n(CO2)]����K�� ��
�����ü�����Ϊȼ�ϵ�ص�ԭ�ϣ���д���ڼ��Խ����е�ظ����ĵ缫��Ӧʽ
����ͨ����ѣ��е�Ϊ-24.9 �棩������Ϊ1.12 L��min-1����״���������Ըõ����Ϊ��Դ���2 mol��L-1 CuSO4��Һ500 mL����ͨ��30 s������������������������ͭ g��
|
|