微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知A~I均为中学化学中的常见物质,它们之间的转化关系如图所示,其中A、D为金属单质,反应过程中需要或生成的水及其他部分产物已略去。请回答以下问题:
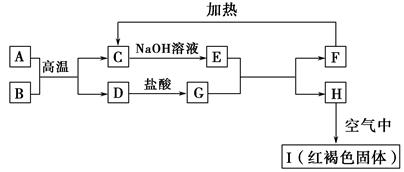
(1)B和F分别是???????????????(填化学式)。
(2)写出下列反应的化学方程式:
①A与B在高温下反应:???????????????????????????????。
②H在空气中转变为I:???????????????????????????????。
(3)E溶液中所有离子浓度由大到小的顺序是???????。
(4)用离子反应方程式表示G溶液呈酸性的原因??????????????????????????????????;该反应的平衡常数为???????(已知常温下,H的溶度积常数Ksp=8.0×10-16)。
2、选择题 下列有关纯铁的叙述正确的是(??)
A.熔点比生铁的低
B.与相同浓度的盐酸反应生成氢气的速率比生铁的快
C.在冷的浓硫酸中可以钝化
D.在潮湿空气中比生铁容易被腐蚀
3、选择题 CuCO3和Cu2(OH)2 CO3的混合物34.6克,可恰好完全溶解于300ml 2 mol・L-1的盐酸中,加热分解等质量的这种混合物可得CuO的质量为?(????)
A.16克
B.19.2克
C.24克
D.30.6克
4、简答题 工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:2FeSO4
??△??
.
?
?Fe2O3+SO2↑+SO3↑.
某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量.
(SO2沸点为-10.02℃)请回答相关问题:
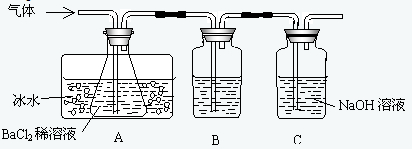
(1)A瓶所盛试剂的作用是______;B瓶所盛的试剂是______;C瓶所盛试剂的作用是______;
(2)A瓶要用冷水冷却的原因是______;
(3)将此反应生成的气体通入A瓶BaCl2溶液中,则______;(填编号)
A.析出BaSO3沉淀???????B.析出BaSO4沉淀???????C.逸出SO3气体????????D.逸出SO2气体
理由是______;
(4)反应后若用A瓶内的混合物来测定已分解的FeSO4的质量,其实验操作的第一步是(简述操作步骤)______.
5、判断题 (15分)已知A为常见的金属单质,根据下图所示的关系:
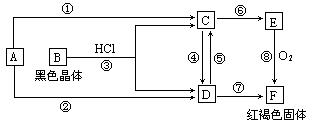
(1)确定A、B的化学式,A为 __________,B为 ___________。
(2)C和D可相互转化,描述C→D溶液的颜色变化:____________________。
④的离子方程式:_____________________________________________________。
⑤的离子方程式:_____________________________________________________。
(3)由E→F的实验现象为:___________________________________。
写出⑧的化学方程式:___________________________________________________。
|