微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 反应:A(s)+B(g)=C(g)在密闭容器中进行,下列情况中,不能使反应速率加快的是 [???? ]
A.升高温度
B.增加A的物质的量
C.使用催化剂
D.压缩
2、简答题 (14分)研究CO2与CH4的反应使之转化为CO和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知:①2CO(g)+O2(g)=2CO2(g) △H=-566 kJ・mol-1
???????????????②2H2(g)+O2(g)=2H2O(g) △H=-484kJ・mol-1
???????????????③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802kJ・mol-1
则CH4(g)+CO2(g)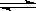 2CO(g)+2H2(g) △H= kJ・mol-1
2CO(g)+2H2(g) △H= kJ・mol-1
(2)在密闭容器中通入物质的量浓度均为0.1mol・L-1的CH4与CO2,在一定条件下发生反应CH4(g)+CO2(g)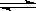 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如下图所示。
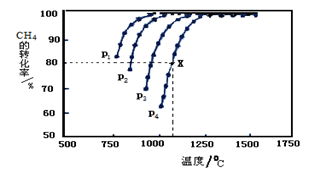
?据图可知,P1、P2、 P3、P4由大到小的顺序 。
?在压强为P4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为???????。该温度下,反应的平衡常数为???????。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g) 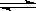 CO(g)+H2 (g)来制取。
CO(g)+H2 (g)来制取。
①在恒温恒容下,如果从反应物出发建立平衡,可认定平衡已达到的是???????
A.体系压强不再变化
B.H2与CO的物质的量之比为1 :1
C.混合气体的密度保持不变
D.气体平均相对分子质量为15,且保持不变
② 在某密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、
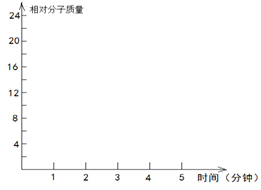
2.2molH2(g)和一定量的C(s),如果此时对体系加压,平衡向????(填“正”或“逆”)反应方向移动,第5min时达到新的平衡,请在下图中画出2~5min内容器中气体平均相对分子质量的变化曲线。
3、简答题 (16分)Ⅰ.硅是信息产业、太阳能电池光电转化的基础材料。锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意图如下:
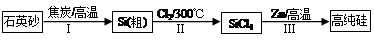
(1)焦炭在过程Ⅰ中做?????剂。
(2)过程Ⅱ中Cl2用电解饱和食盐水制备,制备Cl2的化学方程式为?????????。
(3)整过生产过程必须严格控制无水。
①SiCl4遇水剧烈水解生成SiO2和一种酸,反应方程式为????????????????。
②干燥Cl2时从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入浓H2SO4中。冷却的作用是????????????????????????。
(4)Zn还原SiCl4的反应如下:
反应①:400℃~756℃,SiCl4(g)+2Zn(l) Si(S)+2ZnCl2(l)??△H1<0
Si(S)+2ZnCl2(l)??△H1<0
反应②:756℃~907℃,SiCl4(g)+2Zn(l) Si(S)+2ZnCl2(g)??△H2<0
Si(S)+2ZnCl2(g)??△H2<0
反应③:907℃~1410℃,SiCl4(g)+2Zn(g) Si(S)+2ZnCl2(g)??△H3<0
Si(S)+2ZnCl2(g)??△H3<0
i. 反应②的平衡常数表达式为?????????????????。
ii. 对于上述三个反应,下列说明合理的是???????????。
a.升高温度会提高SiCl4的转化率???? b.还原过程需在无氧的气氛中进行
c.增大压强能提高反应速率????????? d.Na、Mg可以代替Zn还原SiCl4
(5)用硅制作太阳能电池时,为减弱光在硅表面的反射,可用化学腐蚀法在其表面形成粗糙的多孔硅层。腐蚀剂常用稀HNO3和HF的混合液。硅表面首先形成SiO2,最后转化成H2SiF6。用化学方程式表示SiO2转化为H2SiF6的过程?????????????????????。
Ⅱ.(1)甲烷、氢气、一氧化碳的燃烧热分别为akJ・mol-1,bkJ・mol-1,ckJ・mol-1,工业上利用天燃气和二氧化碳反应制备合成气(CO、H2),其热化学反应方程式为??????????????????????。
(2)已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,三种难溶盐的饱和溶液中,Ag+浓度大小的顺序为???????????????。
4、选择题 用铁片与稀硫酸反应制取氢气时,下列措施不能使生成氢气的速率加快的是( )
A.加热
B.降温
C.滴加少量CuSO4溶液
D.不用铁片,改用铁粉
5、选择题 在恒容密闭容器进行的可逆反应:MgSO4(s) + CO(g)  ?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
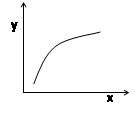
A.若平衡常数K值变大,平衡移动时v逆先减小后增大
B.容器中固体物质的质量不再改变,则反应到达平衡状态
C.若x表示温度,y可表示平衡时混合气体的密度
D.若x表示CO物质的量,y可表示平衡时CO2与CO物质的量之比