��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��12�֣��г��ϳ��۵ġ��ȷ��������Ҫ�ɷ�����м��̿�ۺ�������NaCl��ˮ�ȡ��ȷ��������ǰ�����ϴ�ʹ֮���������������ʱ�������ϴ�������꣬�ͻ�ų�������ʹ����ᷢ�ִ����������������ɡ��ش�:
��1���ȷ���ų���������Դ��_________�ų���������
��2��̿�۵�������________________________��
��3������NaCl��������________________________��
��4��д���йص缫��Ӧʽ�ͻ�ѧ����ʽ________________��
�ο��𰸣��� 12 �֣���1����м������?��2��C��Fe��NaCl��ˮ
�����������
�����Ѷȣ�һ��
2������� ��7�֣����о���ѧ��Ӧ�е������仯ʱ������ͨ���������ʵ�飺
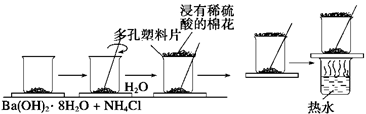
��һ��С�ձ������20 g����ĥ�ɷ�ĩ��Ba(OH)2��8H2O����С�ձ����������ѵ���3��4��ˮ�IJ���Ƭ�ϣ�Ȼ�����ձ��м���Լ10 g NH4Cl���壬����ʵ�鲽�裬��д�±������ش����⡣
ʵ�鲽��
| ʵ��������
|
�������ϣ��������ٽ���
| �д̼�����ζ��ʹʪ�����ɫʯ����ֽ������___��__����
|
�������ձ��²�
| �о��ձ�����˵���˷�Ӧ��_ ��?��Ӧ
|
���������ձ�
| �ձ�����Ĵ��м���ˮ�IJ���Ƭճ�����ձ��ײ�
|
��ճ�в���Ƭ���ձ�����ʢ����ˮ���ձ���
| ����Ƭ���������ձ��ײ�
|
��Ӧ�����߶������Ƭ�۲췴Ӧ��
| �����ɺ�״��֤����_��___����
��1��д����Ŀ�Т٢ڢ����������
��???????????????????��???????????????????��???????????????????
��2��ʵ����Ҫ�����ò�����Ѹ�ٽ����ԭ���ǣ� __________________����2�֣�
��3��������ʵ������У�Ϊʲô�ý���ϡ�����ʪ�����ڶ�����ϰ��ϣ���2�֣�
___________________________________________________________��
�ο��𰸣���1���� NH3�������ȣ���ˮ��
��2��ʹ��Ӧ��Ѹ�ٻ�
���������
�����������1��Ba��OH��2?8H2O��NH4Cl��Ӧ�Ļ�ѧ����ʽΪ��BaCl2?8H2O+2NH4Cl�TBaCl2+2NH3?H2O+8H2O���ٽ������ϣ��������ٽ��裬Ba��OH��2?8H2O��NH4Cl��Ӧ�������д̼�����ζ��ʹʪ�����ɫʯ����ֽ�����İ��������������ձ��²�����о����ձ�������˵���÷�ӦΪ���ȷ�Ӧ���۷�Ӧ�����߶������Ƭ�۲췴Ӧ������ɺ�״��˵��Ba��OH��2?8H2O��NH4Cl�ķ�Ӧ����ˮ���ɣ���2��Ϊ��ʹ��Ӧ��Ѹ�ٻ�϶���ַ�Ӧ��ʹ�¶�Ѹ���½����Ӷ�ʹ��Ӧ�����
�����Ѷȣ�һ��
3��ѡ���� ����˵��������ǣ�������
A����Ӧ��������������������������
B��ʹ�ú��ʵĴ����������¶Ⱦ��ɼӴ�Ӧ����
C������H2Ũ�ȿ���ʹCOȫ����Ӧ
D����Ӧ�ﵽƽ��ʱ������Ӧ���淴Ӧ�Ļ�ѧ��Ӧ��������Ҳ�Ϊ��
�ο��𰸣�A������������������ڷ�Ӧ���������ķ�Ӧ���Ƿ��ȷ�Ӧ��������
���������
�����Ѷȣ�һ��
4��ѡ���� ����Zn(s)+H2SO4(l)=ZnSO4(l)+H2(g)����H ��0 �Ļ�ѧ��Ӧ������������ȷ����(???? )
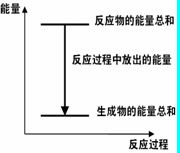
A����Ӧ������������ϵ������ͼ��ʾ
B�������÷�Ӧ��Ƴ�ԭ���пΪ����
C����H��ֵ�뷴Ӧ����ʽ�ļ���ϵ����
D�����������Ϊԭ��ص���32.5gп�ܽ�ʱ��
�����ų�����һ ��Ϊ11.2L
�ο��𰸣�C
���������A��ȷ�����ڦ�H ��0 ������ӦΪ���ȷ�Ӧ�����Է�Ӧ����������������������������B��ȷ��п�ڷ�Ӧ��Ԫ�ػ��ϼ����ߣ���������Ƴ�ԭ���ʱ��пΪ������C������ѧ����ʽ�еĻ�ѧ��������ʾ��Ϊ���ʵ����������릤H��ֵ�����ȣ�D��ȷ�������ܷ�Ӧ����ʽ�����������Ϊԭ��ص���32.5gп�ܽ�ʱ�������ų�����һ ��Ϊ11.2L��
�����Ѷȣ�һ��
5������� ��4�֣���ҵ���ó�����������������ѡ��Ļ�ԭ����C��H2��������ѧ��֪ʶ�жϣ�
��֪��Fe2O3(s)+3/2C(s)=2Fe(s)+3/2CO2(g)?? ��H=+233.8kJ��mol-1??? ��S=279J?K-1?mol-1
Fe2O3(s)+3H2(g)=2Fe(s)+3H2O(g)????��H=+98kJ��mol-1?????��S=144.2J?K-1?mol-1
�ʣ���һ�ֻ�ԭ����ʹ��Ӧ�Է����е��¶ȵͣ���Ҫ�������̣���������λ��Ч���֣�
�ο��𰸣�������Ϊ��ԭ������Ӧ�Է����е��¶Ƚϵ�
���ݦ�H-T��
�����������
�����Ѷȣ���
|