微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关化学实验表现的内容错误的是( )
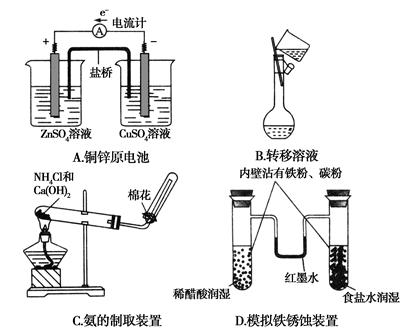
参考答案:A
本题解析:由A项两烧杯中的溶液可推知:盛放硫酸锌溶液的烧杯中的电极应为锌棒,盛放硫酸铜溶液的烧杯中的电极应为铜棒。由原电池原理判断:锌棒应为负极,铜棒应为正极,故A不正确。
本题难度:一般
2、填空题 (10分)下图是一个化学过程的示意图。

(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH的电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出1.6g某金属,则丙中的某盐溶液可能是 (填序号)
A.MgSO4
B.CuSO4
C.NaCL
D.AgNO3
参考答案:(10分)
(1)电解池 (1分)
(2)&#
本题解析:
试题分析:(1)由图可知甲池能自发发生氧化还原反应,是燃料电池,乙、丙都是电解池装置;
(2)甲池通入甲醇的一极是负极,氧气一极是正极,d与负极相连,所以d是阴极,则c是阳极;
(3)通入甲醇的一极是负极发生氧化反应,失去电子生成二氧化碳,二氧化碳与电解质溶液反应,最终生成碳酸根离子和水,电极反应式为CH3OH+8OH--6 e- CO32-+6H2O;
(4)乙是电解硝酸银溶液,A是阳极,B是阴极,所以阳极产生氧气,阴极产生Ag,离子方程式为4Ag++2H2O 4Ag+O2↑+4H+;
4Ag+O2↑+4H+;
(5)乙中B增加的质量是析出的Ag的质量,所以析出5.4gAg时转移电子的物质的量是5.4g/108g/mol=0.05mol,根据反应O2+4e-+2H2O=4OH-,可知甲池中理论消耗氧气得物质的量是0.05/4mol,标准状况下的体积是0.05/4mol×22.4L/mol=0.28L=280mL;丙池析出金属0.64g,丙池转移电子的物质的量也是0.05mol,若该金属是+1价,则该金属的相对原子质量是1.6/0.05=32,若该金属是+2价金属,则该金属的相对原子质量是1.6/0.05/2=64,所以答案选B。
考点:考查原电池、电解池的判断,电化学原理的应用
本题难度:一般
3、选择题 如图所示为普通锌锰电池(即干电池)的组成和结构示意图,其中MnO2的作用是吸收正极放出的H2,下列说法正确的是( )
A.锌是正极,MnO2是负极
B.锌是负极,MnO2是正极
C.锌是正极,石墨棒是负极
D.锌是负极,石墨棒是正极
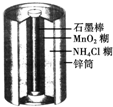
参考答案:普通干电池的电极分别为碳棒和锌筒,以糊状NH4Cl和ZnCl
本题解析:
本题难度:一般
4、填空题 甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为: CO(g)+2H2(g)  CH3OH (g) △H 1(反应Ⅰ)
CH3OH (g) △H 1(反应Ⅰ)
该反应的原料CO和H2本身都可作为燃料提供动力,已知这两种物质燃烧的热化学方程式为:
CO(g)+ O2(g)=CO2(g) △H 2=-283 kJ・mol-
O2(g)=CO2(g) △H 2=-283 kJ・mol- 1 (反应Ⅱ)
1 (反应Ⅱ)
H2(g)+ O2(g)=H2O(g) △H3=-242 kJ・mol-1 (反应Ⅲ)
O2(g)=H2O(g) △H3=-242 kJ・mol-1 (反应Ⅲ)
某些化学键的键能数据如下表: