��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��NA���������ӵ�������ֵ������˵����ȷ����
A�������22.4 L����������̼ԭ����Ϊ6NA
B��84 g NaHCO3�������NA��������
C��1mol �������飩�к���6 NA���ۼ�
�������飩�к���6 NA���ۼ�
D�������22.4 LCl2ͨ������H2O�г�ַ�Ӧ��ת�Ƶ�����ΪNA
�ο��𰸣�B
���������A����ȷ����״���£����鲻����̬����������������Ħ�������̼�������о������������ӵĸ���֮����1�U1������B��ȷ��C����ȷ����Ϊ����12molC��H����������ˮ�ķ�Ӧ�ǿ��淴Ӧ��ת���ʴﲻ��100����D����ȷ����ѡB��
�����Ѷȣ�һ��
2��ѡ���� 2molCl2��2molCO2��Ƚ���ȷ����???????????????????????????????
A�����������
B��ԭ�������
C��������
D���������
�ο��𰸣�A
�������������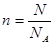 ��֪������ͬ�����£���ͬ���ʵ������κ����庬����ͬ�ķ���������ѡ��A��ȷ��������CO2��ԭ������ͬ��Ħ������Ҳ��ͬ��BD������ȷ�������¶Ⱥ�ѹǿ��һ����ͬ�����������һ����ͬ��CҲ����ȷ����ѡA��
��֪������ͬ�����£���ͬ���ʵ������κ����庬����ͬ�ķ���������ѡ��A��ȷ��������CO2��ԭ������ͬ��Ħ������Ҳ��ͬ��BD������ȷ�������¶Ⱥ�ѹǿ��һ����ͬ�����������һ����ͬ��CҲ����ȷ����ѡA��
�����Ѷȣ���
3��ѡ���� ����ͬ�����Ķ������������������˵�����й�ϵ����ȷ����( )
A������ԭ�ӵĸ�����Ϊ2��3
B������Ԫ�ص�������Ϊ5��4
C������Ԫ�ص�������Ϊ6��5
D������ԭ�ӵĸ�����Ϊ1��1
�ο��𰸣�B
�����������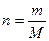 ֪��n(SO2)��n(SO3)=
֪��n(SO2)��n(SO3)=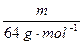 ��
��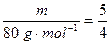 ��
��
A��SO2��SO3����ԭ�ӵĸ�����Ϊ��2��5��3��4=5��6��
B��SO2��SO3�к���Ԫ�ص����ʵ���֮�ȵ�������֮�ȣ�������5��4��
C��SO2��SO3�к���Ԫ�ص������ȵ������ʵ����ȣ�������5��6��
D�����������Ϊ5��4��
�����Ѷȣ�һ��
4�������� ��7�֣����ⶨij��������Ҫ�ɷ�������������������̼������ɣ�����������ʵ�飺��ȡ��ĩ״��Ʒ8.50�ˣ�����ijŨ�ȵ�����100 mL ����ַ�Ӧ���ռ�����״��������2.24 L ��Ȼ��������Ʒ�м���ͬŨ�ȵ�����100mL ����ַ�Ӧ�����ռ�����״��������1.12 L ��
����д�����������̣�
��1����ȡ��������ʵ���Ũ�ȡ���2����������Ʒ��̼����������������3λ��Ч���֣���
�ο��𰸣���1��? 2mol/L????????��2��? 98.8��
���������
���������Fe+2HCl=FeCl2+ H2��.����ǰ�����μ�����������ʵ�����ȣ��ų�����������ڶ����٣�˵���ַų�����1.12L�������е�Fe�Ѿ���Ӧ��ȫ��������������һ����Fe������������������ݻ�ѧ����ʽ��֪��n(HCl)="2" n(H2)="2��(2.24L��22.4L/mol)=0.2mol.C(HCl)=n/V=0.2mol." ��0.1L="2mol/L." n(H2)��=3.36L��22.4L/mol=0.15mol.��n(Fe)= n(H2)=" 0.15mol.,m(F
�����Ѷȣ�һ��
5��ѡ���� ��NA��ʾ�����ӵ�������ֵ��������������ȷ����
A��78 g ������̼̼˫������ĿΪ3NA
B�����³�ѹ�£�22��4 L������̼���е�ԭ������Ϊ3NA
C��1 L 1 mol��L-1��NaClO ��Һ�к���ClO������ĿΪNA
D��1 mol Fe������ϡHNO3��Ӧ��ת��3 NA������
�ο��𰸣�D
���������
���������A���������в�����̼̼˫��������B�����³�ѹ�¡�22��4LCO2�����ʵ�������1mol������D������������ǿ�������Σ�����ˮˮ�⣬��1 L 1 mol��L-1��NaClO ��Һ�к���ClO������ĿС��NA������D�������������������Ϊ�����ӣ�����1 mol Fe������ϡHNO3��Ӧ��ת��3 NA�����ӣ���ȷ����ѡD��
���㣺���鰢��٤�������ļ���
�����Ѷȣ�һ��