微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 【化学--选修3:物质结构与性质】
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
B元素原子的核外p电子数比s电子数少1
C原子的第一至第四电离能分别是:
I1=738kJ/molI2=1451kJ/molI3=7733kJ/molI4=10540kJ/mol
D原子核外所有p轨道全满或半满
E元素的主族序数与周期数的差为4
F是前四周期中电负性最小的元素
G在周期表的第七列
(1)G位于______族______区,价电子排布式为______.
(2)B基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈______
形.
(3)画出C原子的电子排布图______.
(4)已知BA5为离子化合物,写出其电子式______.
(5)DE3中心原子的杂化方式为______,用价层电子对互斥理论推测其空间构型为______.
(6)用电子式表示F元素与E元素形成化合物的形成过程______.
2、选择题 氟的电负性为4.0,另一种元素的电负性为3.5,则这种元素原子的得电子能力比氟原子的得电子能力? [???? ]
A.大
B.小
C.相等
D.无法确定
3、选择题 关于电负性的叙述正确的是 [???? ]
A.同族元素原子序数越大,电负性数值越大
B.除稀有气体外,同周期元素原子序数越大,电负性数值越大
C.电负性数值以F=4.0最大,因其最易失去电子
D.电负性数值大者金属性较强,电负性数值小者非金属性较强
4、选择题 气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位: eV(电子伏特)]数据。
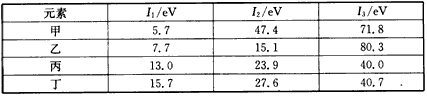
下列说法正确的是 [???? ]
A.甲的金属性比乙强
B.乙的化合价为+1价
C.丙一定为非金属元素
D.丁一定是金属元素
5、填空题 已知元素原子的电负性和原子半径等一样,也是元素的一种基本件质,下列给出14种元素的电负性

试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是_____________。
(2)由上述变化规律可推断,短周期主族元素中,电负性最大的元素是____________,电负性最小的元素是__________,由这两种元素构成的化合物属于___________(用“离子”或“共价”填空)化合物,并用电子式表示该化合物的形成过程:__________________
|