微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列四种有色溶液与SO2作用,均能褪色。其实质相同的是( )
①品红溶液?????????????????? ②酸性KMnO4溶液????
③溴水???????????????????④滴有酚酞的NaOH溶液 ????
A.①④
B.①②③
C.②③
D.②④
参考答案:C
本题解析:
试题分析:SO2使品红溶液褪色,利用的是SO2与有色物质的化合作用;使酸性高锰酸钾溶液和溴水褪色,利用的是SO2的还原性;使滴有酚酞的NaOH溶液褪色,利用的是SO2是酸性氧化物的通性,所以答案选C。2化学性质的有关判断
点评:该题是高考中的常见考点之一,属于基础性试题的考查,难度不大。该题的关键是记住SO2的化学性质,并能结合题意做到具体问题、具体分析即可,有利于培养学生的逻辑推理能力,提高学生的学习兴趣和学习积极性。
本题难度:简单
2、选择题 下列关于SO2性质的说法中,不正确的是
A.能使品红溶液褪色
B.能与水反应生成硫酸
C.能与NaOH溶液反应
D.能使酸性KMnO4溶液褪色
参考答案:B
本题解析:
试题分析:A.SO2有漂白性,能使品红溶液褪色。正确但不符合题意。B .SO2与水发生反应产生亚硫酸。错误,符合题意。C. SO2是酸性氧化物,与碱发生反应SO2+2NaOH=Na2SO3+H2O. 正确但不符合题意.D.SO2有还原性,能被高锰酸钾溶液氧化: 2KMnO4+5SO2+2H2O= K2SO4+ 2MnSO4 + 2H2SO4。能使酸性KMnO4溶液褪色.正确但不符合题意。选项为B.2的性质。
本题难度:一般
3、选择题 下列关于浓硫酸的叙述中,正确的是
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸具有强氧化性,常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸具有脱水性,常用作气体的干燥剂
D.浓硫酸具有强氧化性,常温下能使铁、铝等金属表面形成氧化膜而钝化
参考答案:D
本题解析:
试题分析:A不正确,炭化利用的是浓硫酸的脱水性;B不正确,浓硫酸与铜反应需要加热;C不正确,浓硫酸作干燥剂,利用的是浓硫酸的吸水性,D正确,答案选D。
点评:该题是中等难度的试题,主要是考查学生对浓硫酸性质的熟悉掌握程度,有助于巩固学生的基础知识,提高学生的应试能力。该题需要注意的是在对硫酸性质的考查中,浓硫酸的三大特性是常考的知识点,尤其是浓硫酸的强氧化性。解题时应多角度分析,防止出现差错。
本题难度:简单
4、实验题 (18分)含硫物质燃烧会产生大量烟气,主要成分是SO2、CO2、N2、O2。某研究性学习小组在实验室利用下列装置制备模拟烟气,并测算模拟烟气通过转化器的脱硫效率。
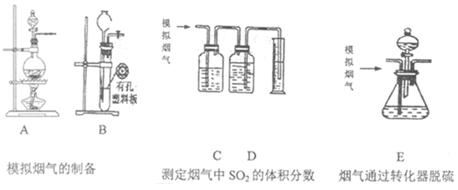
回答下列问题:
I.模拟烟气的制备
(1)用A装置制SO2,其化学反应方程式为??????????????????。
(2)用B装置制CO2,使用该装置优点的是??????????????????????。
(3)将制得的气体与空气充分混合,获得模拟烟气用于后续实验。
II.测定烟气中SO2的体积分数
(4)将部分模拟烟气缓慢通过C、D装置,其中C、D中盛有的药品分别是??????、??????。(填序号)
①KMnO4溶液? ②饱和NaHSO3溶液? ③饱和Na2CO3溶液? ④饱和NaHCO3溶液
(5)若模拟烟气的流速为a mL/min,若t1分钟后,测得量简内液体体积为V mL(已折算为标准状况),则SO2的体积分数是??????????。
III.测算模拟烟气通过转化器的脱硫效率(已转化的SO2占原有SO2的百分比)
(6)将模拟烟气通过转化器E装置,E装置中盛有FeCl2、FeCl3的混合溶液,常温下,它可催化SO2与O2的反应,以达到脱硫目的。写出SO2与FeCl3溶液参与反应过程的离子方程式????????????。
(7)若模拟烟气仍以a mL/min的流速通过转化器E装置,t2分钟后,向E装置中加入酸化的BaCl2溶液得到白色浑浊液,经?????、洗涤、??????、称量,得到mg固体。若实验的气体体积已折算为标准状况,则该转化器的脱硫效率是??????????。
参考答案:I.(1)Cu + 2H2SO4(浓) 本题解析:
本题解析:
试题分析:(1)装置A需要加热,这说明所用试剂是浓硫酸和铜,反应的化学方程式为Cu + 2H2SO4(浓) CuSO4 + 2H2O + SO2↑。
CuSO4 + 2H2O + SO2↑。
(2)B装置制CO2,属于简易启普发生器,使用该装置优点的是通过控制长颈漏斗盐酸的加入量,控制反应的发生和停止。
Ⅱ.(4)二氧化硫具有强的还原
本题难度:一般
5、选择题 下表所列举的各组事实中,存在因果关系的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A、从工业生产硫酸用浓硫酸吸收分析;
B、从氯气和二氧化硫的性质分析,混合通入水溶液中反应;
C、从金属性的强弱取决于失电子的能力分析;
D、从石墨的化学性质和导电性分析.
解答:A、三氧化硫易和水反应,但在工业制硫酸中用水吸收三氧化硫易形成酸雾,阻止吸收,所以用98.3%的浓硫酸吸收三氧化硫,无因果关系,故A不选;
B、氯气与水反应生成的次氯酸有漂白作用,二氧化硫有漂白作用,但二者在水的作用下反应生成生成硫酸和盐酸,Cl2+SO2+2H2O=H2SO4+2HCl,Cl2和SO2混合后不能用于漂白纸浆,无因果关系,故B不选;
C、金属性的强弱是由失电子能力决定的,钠失电子能力强于铝,所以钠的金属性强于铝,与铝最外层电子数多无关,无因果关系,故C不选;
D、石墨具有良好的导电性,化学性质稳定一般不发生反应,可以做电解池中的电极,所以前后有因果关系,有因果关系,故D选;
故选D.
点评:本题主要考查物质的性质和用途,解答时要充分理解各种物质的性质,然后再根据物质的性质方面进行分析、判断,从而确定物质的用途.
本题难度:困难