微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在硫酸工业生产中,SO3的吸收过程是在吸收塔(如右图)中进行的,吸收塔里还装入大量瓷环。下列有关说法中,不正确的是

A.从①处通入含SO3的混合气体,整个吸收操作采取逆流的形式
B.从②处喷下98.3%的硫酸,瓷环的作用是增大接触面积
C.从③处导出的尾气中含量最高的气体是SO2,所以不可直接排入大气
D.从④处流出的是可用水或稀硫酸稀释的“发烟”硫酸
参考答案:C
本题解析:在硫酸工业生产中,为了使SO3的吸收充分,采取逆流的形式,A正确;在吸收塔中装有瓷环,其目的是增大浓硫酸与SO3的接触面积,使SO3尽可能被浓硫酸吸收,B正确,从③处导出的尾气中含量最高的气体是N2,同时还含有未反应完全的SO2、SO3、O2等气体,所以不可直接排入大气中,C错;SO3被浓硫酸吸收后,硫酸成为“发烟硫酸”,此时的“烟”实际上是雾,硫酸小液滴,但是习惯上人们将其称为“烟”,D正确。
本题难度:一般
2、选择题 将BaCl2溶液分盛两支试管,第1支加入HNO3,第2支加入烧碱溶液,然后再分别通入SO2气体,结果两试管均有白色沉淀产生。下列说法正确的是???????????????????????????????(???)
A.证明SO2具有强氧化性和酸性
B.若第1支试管改通H2S或Cl2溶解,后再通SO2气体,均不会产生沉淀
C.若第2支试管改通NH3,后通SO2,不会产生沉淀
D.升高pH使SO2水溶液中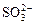 浓度增大
浓度增大
参考答案:D
本题解析:略
本题难度:简单
3、选择题 全社会都在倡导诚信,然而总是有一部分不法商贩却在背道而驰。如有些商贩为了使银耳增白,就用硫磺(燃烧硫磺)对银耳进行熏制,用这种方法制取的洁白的银耳对人体是有害的。这些不法商贩所制取的银耳是利用了?(???)。
A.S的漂白性
B.S的还原性
C.SO2的漂白性
D.SO2的还原性
参考答案:C
本题解析:
试题分析:硫磺燃烧生成SO2,SO2具有漂白性,答案选C。2漂白性的熟悉了解程度,试题贴近生活实际,有利于培养学生的逻辑推理能力,增强学生的社会责任感。
本题难度:简单
4、填空题 有黑色和黄色两种固体物质A和B,它们都是由相同的两种元素组成.A与稀 作用产生气体C,B在充足的空气中燃烧生成气体D,C和D的水溶液都呈酸性,并都能使溴水褪色,且C和D混合后不久有固体物质E生成.
作用产生气体C,B在充足的空气中燃烧生成气体D,C和D的水溶液都呈酸性,并都能使溴水褪色,且C和D混合后不久有固体物质E生成.
(1)由A生成C的离子方程式是________________________
(2)B燃烧生成D的化学方程式是________________________
(3)C和D混合后反应的化学方程式是________________________
参考答案:① 本题解析:此题是一道根据性质进行推断的题目,此题的突破口是“C和D的水溶液都显酸性,并都能使溴水褪色”,可知C为
本题解析:此题是一道根据性质进行推断的题目,此题的突破口是“C和D的水溶液都显酸性,并都能使溴水褪色”,可知C为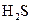 ,D为
,D为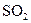 ,A为
,A为
本题难度:简单
5、实验题 现有某铁碳合金(铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究。
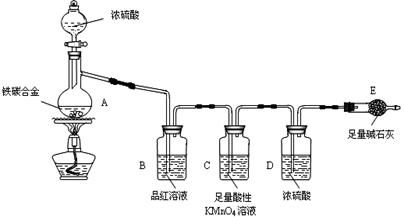
I?测定铁的质量分数:
(1)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根导管,然后__________________________________,则证明装置的气密性良好。
(2)称量E的质量,并将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为__________________________(写表达式)。
(3)装置C的作用______________________________________________。
(4)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是___________________________________________________________。
(5)乙同学按照甲同学认为改进实验,改进方法是______________但测得合金中铁的质量分数却偏高。你认为其中可能的原因是_________________。
Ⅱ?探究浓硫酸的某些性质:
(6)往A中滴加足量的浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:________________________________________________。
(7)A中铁与浓硫酸发生反应的化学方程式是_______________________。
参考答案:(1)把导管放入盛有水的水槽中,微热烧瓶,如果导管口有气泡产
本题解析:
试题分析:(2)在装置A中发生Fe和C与浓硫酸的反应,产生CO2、SO2和铁的氧化物,装置B检验SO2,装置C吸收SO2,装置D干燥气体的,装置E是吸收CO2的,E增重的质量b是CO2的质量。
C---------CO2
1??????????????1
b/44?? b/44? C的质量:12b/44="3" b/11? Fe质量分数:(a-3 b/11)/a)×100%= 本题难度:一般
本题难度:一般