微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中所含分子物质的量最多的是
A.4℃时2.7mL 水
B.2.24L一氧化碳(标准状况下)
C.6.02×1022个氯化氢分子
D.4.9g磷酸
参考答案:A
本题解析:
试题分析:A中水的物质的量是2.7g÷18g/mol=0.15mol;B中,CO的物质的量是2.24L÷22.4L/mol=0.1mol;C中;氯化氢的物质的量是6.02×1023÷6.02×1023/mol=1.0mol;4.9g磷酸的物质的量是4.9g÷98g/mol=0.05mol,答案选A。
点评:在进行物质的量的有关计算时,关键是熟练应用几个关系式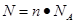
本题难度:一般
2、选择题 取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol・L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是(????)
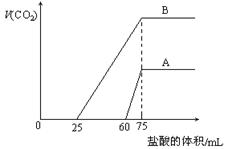
A.原NaOH溶液的物质的量浓度为0. 5mol/L
B.A线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3,NaHCO3
C.B线中消耗盐酸0 < v(HCl) < 25mL时发生的离子反应为: OH-+H+=H2O? H++CO32-=HCO3-
D.B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为112mL
参考答案:D
本题解析:
试题分析:观察图象,B曲线不产生气体需要盐酸的体积少于产生气体需要盐酸的体积,B曲线为Na2CO3和NaHCO3混合溶液,A曲线不产生气体需要盐酸的体积多于产生气体需要盐酸的体积,A曲线为Na2CO3和NaOH混合溶液。B错误。
B线中消耗盐酸0 < v(HCl) < 25mL时发生的离子反应为:H++CO32-=HCO3-,C错误;
无论A曲线或B曲线,当加入盐酸75mL时,产生二氧化碳气体体积最大,此时恰好完全反应,溶液中溶质为NaCl,Na+来自氢氧化钠,Cl-来自盐
本题难度:一般
3、选择题 用NA表示阿伏加德罗常数,下列说法中正确的是(??)
A.84 g NaHCO3晶体中含有NA个CO32-
B.9.2 g NO2和N2O4的混合气中含有的氮原子数为0.2NA
C.标准状况下,11.2 L臭氧中含NA个氧原子
D.78 g Na2O2与足量的CO2反应,电子转移个数为2NA
参考答案:B
本题解析:A项,在NaHCO3晶体中不存在CO32-;C项,在标准状况下,11.2 L O3中含1.5NA个氧原子;D项,78 g Na2O2与足量CO2反应,电子转移个数为NA。
本题难度:一般
4、简答题 化学计量在化学中占有重要地位,请回答下列问题:
(1)0.3molNH3分子中所含原子数与______个H2O分子中所含原子数相等.
(2)含0.4molA13+的Al2(SO4)3中所含的SO42-的物质的量是______.
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为______.
(4)在一定的温度和压强下,1体积气体X2 跟3体积气体Y2 化合生成2体积化合物,则该化合物的化学式是______.
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol?L-1、0.25mol?L-1、0.4mol?L-1,则c(SO42-)=______.
参考答案:(1)0.3molNH3分子中所含原子数为0.3×4NA=1
本题解析:
本题难度:简单
5、选择题 把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为(? )
A.(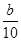 -
-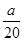 ) mol/L
) mol/L
B.(2b-a) mol/L
C.(5b-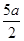 ) mol/L
) mol/L
D.(10b-5a) mol/L
参考答案:D
本题解析:设五等份NH4HCO3和Na2CO3的混合溶液中NH4HCO3和Na2CO3的量均分别为x mol,y mol,可列出方程组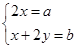 ,则可解得n(Na+)=(b-a/2) mol,从而可求出该混合溶液中,c(Na+)=(10b-5a) mol/L,D项正确。
,则可解得n(Na+)=(b-a/2) mol,从而可求出该混合溶液中,c(Na+)=(10b-5a) mol/L,D项正确。
本题难度:一般