微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列变化过程属于氧化反应的是[???? ]
A. HCl→H2
B. Mg→Mg2+
C. Cl-→AgCl
D. CuO→Cu
2、选择题 下列的氧化还原反应中,水既不是氧化剂也不是还原剂的是
A.2Na+2H2O=2NaOH+H2↑
B.2F2+2H2O=4HF+O2↑
C.CaO+H2O=Ca(OH)2
D.Cl2+H2O=HCl+HclO
3、填空题 (8分)现有①KMnO4?②H2?③O2?④CL2?⑤CO?⑥AL 六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲:_____ 中,常用的还原剂放入乙:_____中,则:
⑴甲中有???????;乙中有???????。(填序号)
⑵由Fe 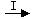 Fe3O4 ,Fe2O3
Fe3O4 ,Fe2O3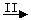 Fe 可知,欲实现I反应过程应从___________?(填“甲”或“乙”,下同)中找物质,欲实现II反应过程应从????????中找物质。
Fe 可知,欲实现I反应过程应从___________?(填“甲”或“乙”,下同)中找物质,欲实现II反应过程应从????????中找物质。
⑶请将4种物质:Fe、Fe2O3、CO、CO2分别填入 下面对应的横线上,组成一个配平了的化学方程式,并标出电子转移的方向和数目。(提示:反应物是Fe2O3和3 CO )
下面对应的横线上,组成一个配平了的化学方程式,并标出电子转移的方向和数目。(提示:反应物是Fe2O3和3 CO )



 +?????????? ="====?????????????" +???????????????????
+?????????? ="====?????????????" +???????????????????
⑷一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
4X+5O2 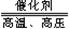 4NO+6H2O,则根据质量守恒定律可以推出X的化学式为????????。
4NO+6H2O,则根据质量守恒定律可以推出X的化学式为????????。
4、填空题 硝酸是一种强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。?实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(1)请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:_____________。
(2)该反应中发生氧化反应的物质是__________,1 mol氧化剂_________(填“得到”或“失去”)_______ mol电子。
(3)48.0 g Cu与适量的浓HNO3反应,铜全部作用后,共收集到22.4 L气体(标准状况下),反应中消耗HNO3的物质的量可能是(???)
A.1.5 mol??????? B.2.0 mol??????? C.2.5 mol??????? D.3.0 mol
(4)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等。请将3种物质: FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
HNO3??+? ______  ???______?+? ______ +? N2O↑ +? H2O
???______?+? ______ +? N2O↑ +? H2O
并写出配平后的离子方程式:_________________________。
(5)硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念――“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是(???)
A.Cu  Cu(NO3)2
Cu(NO3)2
B.Cu 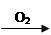 CuO
CuO Cu(NO3)2
Cu(NO3)2
C.Cu 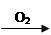 CuO
CuO Cu(OH)2
Cu(OH)2 Cu(NO3)2?????
Cu(NO3)2?????
D.Cu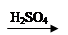 CuSO4
CuSO4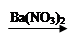 Cu(NO3)2
Cu(NO3)2
5、选择题 下列褪色过程不是因为氧化还原反应而褪色的是(??)
A.SO2气体通入到溴水中使溴水褪色
B.氯水使滴有酚酞的NaOH溶液褪色,再加入NaOH后不变红
C.SO2气体能使品红溶液褪色
D.在含有碘单质的淀粉溶液中,加入KOH溶液后蓝色褪去