微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.热化学方程式C2H2(g)+5/2O2(g)=2CO2(g)+H2O(g)△H=-1256kJ/mol,表示乙炔的燃烧热为1256kJ/mol
B.―OH与OH-组成元素相同,含有的电子数也相同
C.H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ /mol,表示含1molNaOH的氢氧化钠溶液与含0.5mol H2 SO4的浓硫酸混合后放出57.3 kJ的热量
D.中和热测定实验中,不能用铜丝搅拌棒代替环形玻璃搅拌棒
参考答案:D
本题解析:
试题分析:A、燃烧热中,H元素对应的温度氧化物是液态水,所以乙炔的燃烧热不是1256kJ/mol,错误;B、羟基的电子数是9,而氢氧根离子中的电子数是10,错误;C、浓硫酸与氢氧化钠反应放出的热量不表示中和热,因为浓硫酸溶于水放热,所以1molNaOH的氢氧化钠溶液与含0.5mol H2 SO4的浓硫酸混合后放出大于57.3 kJ的热量,错误;D、铜是金属,易导热,用铜丝搅拌棒会造成热量的散失,影响实验结果,所以中和热测定实验中,不能用铜丝搅拌棒代替环形玻璃搅拌棒,正确,答案选D。
考点:考查燃烧热、电子数、中和热的的判断极中和热测定实验的判断
本题难度:一般
2、选择题 下列说法中,正确的是
A.中和反应是放热反应,盐类水解反应是吸热反应
B.1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热
C.在101 kPa时,1 mol碳燃烧所放出的热量一定叫碳的燃烧热
D.CO燃烧是吸热反应
参考答案:A
本题解析:
试题分析:A.中和反应是放热反应,盐类水解反应是吸热反应,正确;B.中和热是指强酸、强碱的稀溶液生成1mol水时放出的热量,1 mol H2SO4与1 mol Ba(OH)2完全中和除生成水外,还生成硫酸钡,错误;C.在101 kPa时,1 mol碳完全燃烧生成稳定氧化物时所放出的热量叫碳的燃烧热,错误;D.CO燃烧是放热反应,错误;选A。
考点:考查燃烧热、中和热等知识。
本题难度:一般
3、选择题 下列描述中正确的是
A.氧化还原反应一定都是放热反应
B.强酸与强碱反应都是放热反应
C.放热反应的反应速率总是大于吸热反应的反应速率
D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的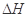 不同
不同
参考答案:B
本题解析:
试题分析:碳与水蒸气反应生成CO和氢气,属于氧化还原反应,也属于吸热反应,A项错误;酸碱中和反应都是放热反应,B项正确;影响化学反应速率的本质因素是物质本身的性质,与反应是否放热无关,C项错误;化学反应的焓变只与反应物与生成物的状态有关,与反应途径和条件无关,D项错误;选B。
考点:考查化学反应的热效应,氧化还原反应的热效应等知识。
本题难度:一般
4、选择题 下列叙述中,正确的是
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.晶体中只要有阴离子就一定有阳离子
D.金属原子失去电子变成稳定结构时吸收的能量越多,则该原子金属性越强。
参考答案:C
本题解析:A:硫离子与钾离子的核外电子排布完全相同,但前者只有还原性,后者只有氧化性;
B:Fe2+的核外最外层电子数为14;
D:金属原子失去电子变成稳定结构时吸收的能量越小,则越易失电子,则该原子金属性越强
本题难度:一般
5、选择题 已知断开1 mol H2中的化学键需要吸收436kJ的能量,断开1 mol Cl2中的化学键需要吸收243kJ的能量,而形成1mol HCl分子中的化学要释放431kJ的能量,则1mol氢气与1mol氯气反应时能量变化为( )
A.吸收183kJ
B.吸收366kJ
C.放出183kJ
D.放出366kJ
参考答案:C
本题解析:
试题分析::H2(g)+Cl2(g)=2HCl(g)的反应热=生成物的键能减反应物的键能=436kJ?mol-1+243kJ?mol-1-2×431 kJ?mol-1=
-183kJ?mol-1,故1mol氢气与1mol氯气反应时放出热量为183KJ,故选C。
考点:有关反应热的计算
点评:本题主要考查了反应热的计算,难度不大,根据课本知识即可完成。
本题难度:一般