微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知299 K时,合成氨反应N2(g)+3H2(g)  2NH3(g)ΔH=-92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应 ,测得反应放出的热量为(忽略能量损失)
2NH3(g)ΔH=-92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应 ,测得反应放出的热量为(忽略能量损失)
A.一定等于92.0 kJ
B.一定小于92.0 kJ
C.一定大于92.0 kJ
D.不能确定
参考答案:B
本题解析:
试题分析:热化学方程式N2(g)+3H2(g)  2NH3(g)ΔH=-92.0 kJ/mol的意义表示1mol N2与3mol H2完全反应生成2mol NH3放出热量为92.0kJ,但实际该反应为可逆反应将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,不会完全,故放出热量一定小于92.0 kJ,故B项正确。
2NH3(g)ΔH=-92.0 kJ/mol的意义表示1mol N2与3mol H2完全反应生成2mol NH3放出热量为92.0kJ,但实际该反应为可逆反应将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,不会完全,故放出热量一定小于92.0 kJ,故B项正确。
考点:热化学方程式意义。
本题难度:一般
2、选择题 下列说法不正确的是
A.在人类研究物质微观结构的过程中,先后使用了光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器
B.铝硅酸盐分子筛可用于物质分离,还可用作干燥剂、催化剂及催化剂载体
C.使用可再生资源、提高原子经济性、推广利用二氧化碳与环氧丙烷生成的可降解高聚物等都是绿色化学的内容
D.铁盐会水解产生具有吸附性的胶体粒子,可用于饮用水的杀菌消毒
参考答案:D
本题解析:
试题分析:A项在人类研究物质微观结构的过程中,先后使用了光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器,A项正确;B项铝硅酸盐形成的分子筛中有许多笼状空穴和通道,常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、催化剂及催化剂载体等,故B项正确;C项“绿色化学”由美国化学会(ACS)提出,目前得到世界广泛的响应。其核心是利用化学原理从源头上减少和消除工业生产对环境的污染;反应物的原子全部转化为期望的最终产物,故使用可再生资源、提高原子经济性、推广利用二氧化碳与环氧丙烷生成的可降解高聚物等都是绿色化学的内容,C项正确;D.铁盐会水解产生具有吸附性的胶体粒子,可用于饮用水的净化处理,但不能用于饮用水的杀菌消毒,故D项错误;本题选D。
考点:化学与生产生活。
本题难度:一般
3、填空题 (12分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
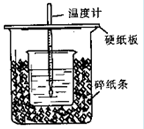
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由 。
参考答案:(1)环形玻璃搅拌棒 (2
本题解析:考查中和热的测定实验。
(1)在反应中为了使反应进行的更充分,同时也为了使溶液混合均匀,需要搅拌。因此还缺少环形玻璃搅拌棒。
(2)该实验应该离开你减少热量的损失,所以烧杯间填满碎纸条的作用是减少实验过程中的热量损失。
(3)大烧杯上如不盖硬纸板,则会导致热量损失,使测定结果偏小。
(4)如果改变酸碱的物质的量,则反应中放出的热量是不相同的,但中和热是不变的,因为中和热是指酸跟碱发生中和反应生成1mol H2O所放出的热量,与酸碱的用量无关。
本题难度:一般
4、选择题 下列物质中,只含有离子键的是
A.HCl
B.CaCl2
C.NH4Cl
D.NaOH
参考答案:B
本题解析:
试题分析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,据此可知选项A中只有共价键,B中只有离子键,C中含有离子键和极性键,D中含有离子键和极性键,答案选B。
点评:该题是高考中的常见考点,属于基础性试题的考查,试题基础性强,侧重对学生基础知识的训练,主要是考查学生灵活运用化学键知识解决实际问题的能力。该题的关键是明确离子键、共价键的含义和判断依据,然后结合题意灵活运用即可。
本题难度:简单
5、填空题 已知:H2(g)+1/2O2(g)=H2O(g),反应过程中能量变化如下图所示,回答:

(1)a、b分别代表的意义是: a______ 化学键时_________的能量; b______化学键时______的能量;
(2)该反应ΔH______0 kJ・mol-1(填“<”或“>”=)。
参考答案:(1)旧键断裂;吸收的能量;生成新键;放出的能量
(
本题解析:
本题难度:一般