微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于化学键的说法中不正确的是( )
A.化学键是一种物质
B.化学键可以使用离子相结合,也可以使原子相结合
C.化学反应中必然有化学键的断裂与形成
D.离子键可以形成离子化合物
参考答案:A.因化学键是一种相邻原子间的强烈的相互作用,则化学键是一种
本题解析:
本题难度:简单
2、选择题 已知:H2O(g)====H2O(l) ΔH=Q1 kJ・mol-1 2H2O(g)====2H2(g)+O2(g)ΔH=Q2 kJ・mol-1 CH4(g)+2O2(g)====CO2(g)+2H2O(l) ΔH=Q3 kJ・mol-1,则H2和CH4的燃烧热的比是
A.(Q1+Q2)/(2Q1+Q3)
B.(Q1-Q3)/(Q3-2Q1)
C.(2Q1+Q2)/2Q3
D.(2Q1-Q2)/2Q3
参考答案:D
本题解析:根据盖斯定律,由第一个反应减去第二个反应的1/2得H2燃烧的热化学方程式:H2(g)+1/2O2(g)====H2O(l) ΔH=Q1-1/2Q2?即H2的燃烧热为(Q1-1/2Q2) kJ・mol-1,由第三个热化学方程式知甲烷燃烧热为Q3 kJ・mol-1,故H2和CH4的燃烧热的比是(2Q1-Q2)/2Q3,答案为D项。
本题难度:简单
3、选择题 下列叙述正确的是
A.熵变小于零而焓变大于零的反应肯定不能发生
B.热化学方程式中ΔH的值与反应物的用量有关
C.化学反应中旧键断裂吸收能量,新键形成释放能量,所以化学反应伴随能量变化,但反应前后物质的总能量不变
D.用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度维持25℃不变,溶液中各离子浓度均减小
参考答案:C
本题解析:
试题分析:A、熵变小于零即△S<0,焓变大于零即△H>0,△G=△H-T△S>0,反应不自发进行,不代表反应不能发生,错误;B、热化学方程式中ΔH的值与反应物的用量无关,与热化学方程式中反应物的系数有关,错误;C、化学反应中旧键断裂吸收能量,新键形成释放能量,但遵循能量守恒定律,反应前后物质的总能量不变,所以化学反应伴随能量变化,正确;D、醋酸的稀释过程中,氢离子、醋酸根离子的浓度减小,但氢氧根离子的浓度增大,错误,答案选C。
考点:考查反应自发的判断,热化学方程式与热效应的关系,溶液稀释过程离子浓度的变化
本题难度:一般
4、选择题 已知1 mol白磷变成1 mol红磷放出18.39KJ热。下列两个反应:4P(白、固)+5O2(气)=2P2O5(固)+Q1,4P(红、固)+5O2(气)=2P2O5(固)+Q2,其中Q1与Q2的关系正确的是??
A.Q1=Q2
B.Q1>Q2
C.Q1<Q2
D.无法比较
参考答案:B
本题解析:由题意可知4P (白、固)=4P(红、固)+Q,则Q1=Q2+Q,因此,答案选B。
本题难度:一般
5、选择题 白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P―P a kJ・mol―1、P―O b kJ・mol―1、P="O" c kJ・mol―1、O=O d kJ・mol―1。根据下图示的分子结构和有关数据估算该反应的△H
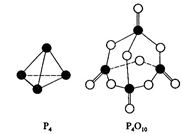
其中正确的是:
A.(4a+5d-4c-12b)kJ・mol―1
B.(4c+12b-4a-5d)kJ・mol―1
C.(4c+12b-6a-5d)kJ・mol―1
D.(6a+5d-4c-12b)kJ・mol―1
参考答案:D
本题解析:
试题分析:反应热=反应物的键能总和-生成物的键能总和,在1摩尔白磷中含有6摩尔化学键,在1摩尔P4O10中有4摩尔P=O,12摩尔P―O,所以反应热为:(6a+5d-4c-12b)。选D。
考点:键能计算反应热。
本题难度:一般