微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于O2+2SO2?2SO3的叙述错误的是( )
A.增加O2的浓度能加快反应速率
B.若O2足量,则SO2可以完全转化为SO3
C.加入催化剂能加快反应速率
D.升高体系温度能加快反应速率
参考答案:A.增加O2的浓度,活化分子的数目增多,能加快反应速率,故A
本题解析:
本题难度:简单
2、选择题 影响活化分子的百分数的因素有( )
①温度②浓度③压强④催化剂⑤接触面积
A①② B、①②③④ C、①④ D、②④
参考答案:C
本题解析:只有温度和催化剂才能增大活化分子的百分数,所以答案选C。
本题难度:一般
3、选择题 亚氯酸钠(NaClO2)是一种性能优良的漂白剂,但遇酸性溶液发生分解: 5HClO2 = 4ClO2↑ + H+ + Cl-+ 2H2O。向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为硫酸,开始时反应缓慢,一段时间产生气体速度较快,速度变化的原因是 [???? ]
A.逸出ClO2使生成物浓度降低
B.酸使亚氯酸的氧化性增强
C.溶液中的H+起催化作用
D.溶液中的Cl-起催化作用
参考答案:D
本题解析:
本题难度:一般
4、选择题 可逆反应mA(g)+nB(s) rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分含量和温度T或压强P关系如图所示,下列叙述中正确的是
rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分含量和温度T或压强P关系如图所示,下列叙述中正确的是
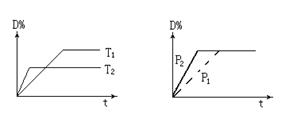
A.化学方程式系数m+n=r+q
B.使用催化剂,D的物质的量分数增加
C.温度降低,化学平衡向正反应方向移动
D.物质B的颗粒越小,反应越快,有利于平衡向正反应方向移动
参考答案:C
本题解析:
试题分析:A.由右图可知,压强为P2先到达平衡,故P2>P1,增大压强,D%不变,则平衡不移动,反应中B为固体,故m=r+q,故A错误;B.使用催化剂,缩短到达平衡时间,平衡不移动,D%的不变,故B错误;C、由左图知,温度T2为先到达平衡,故T2>T1,升高温度,D%减小,则平衡向逆反应移动,因此温度降低,化学平衡向正反应方向移动,C正确;D.B为固体,物质B的颗粒越小,接触面积越大,反应越快,但对平衡移动没有影响,故D错误,故选C。
考点:考查化学平衡的移动、化学平衡影响因素、化学平衡图象等
本题难度:一般
5、选择题 用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,为了加快化学反应的反应速率,下列措施你认为可行的是
A.加入蒸馏水
B.加热
C.加入NaCl溶液
D.加入浓盐酸
参考答案:BD
本题解析:加入蒸馏水,稀释盐酸,则反应速率减慢;
加热,即升温,则反应速率加快;
加入NaCl溶液,同A,相当于稀释盐酸,则反应速率减慢;
加入浓盐酸,即增大盐酸浓度,则反应速率加快;
本题难度:一般