��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��14�֣����ǵؿ��к�����ߵĽ���Ԫ�أ��䵥�ʡ��Ͻ��仯���������������е�Ӧ�������㷺�������������������仯�������Ҫԭ�ϡ�
��1����Ԫ����Ԫ�����ڱ��е�λ���� ��
��2�������������Խ����һ����������价������ȫ���ܵ�Խ��Խ��Ĺ�ע����ԭ����ͼ��ʾ��
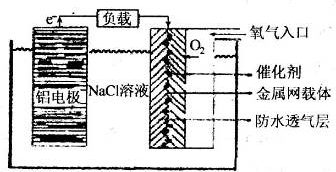
�ٸõ�ص��ܷ�Ӧ��ѧ����ʽΪ ��
�ڵ����NaCl�������� ��
������һ�������Ϊ��Դ���KI��Һ��ȡKIO3��ʯīΪ�缫���ϣ�ʱ���������������ĵ缫��ӦʽΪ ��
��ij��һ������ص�Ч��Ϊ50%������������Դ���500mL�ı���NaCl��Һ����������������Һ��������Һ���ǰ��������䣩��NaOH��Ũ��Ϊ0.3 mol��L��1����ù�����������������Ϊ ��
��3���Ȼ����㷺�����л��ϳɺ�ʯ��ҵ�Ĵ��������Ȼ���Ҳ�����ڳ�����ˮ������
���Ȼ����ڼ�������������������̬�Ȼ����Ļ�ѧʽΪAl2Cl6��ÿ��Ԫ�ص�ԭ���������ﵽ8�����ȶ��ṹ������ṹʽΪ ��
�ڽ����������̼�ۻ�Ϻ���Ȳ�ͨ���������ɵõ��Ȼ�����ͬʱ����CO��д���÷�Ӧ�Ļ�ѧ����ʽ ��
�ο��𰸣���1�����������ڵڢ�A�壨2�֣�
��2������4Al+3
���������
�������������1������Ԫ�غ˵����Ϊ13���ڵ������ڵ�IIIA�壻��2�����ٿ�����������ˮ������Ӧ����������������Ӧ����ʽΪ��4Al+3O2+6H2O=4Al(OH)3������Һ������Ũ��Խ�������������Խ�࣬��Һ�ĵ�����Խǿ�������Ȼ��ƣ������������ƶ����ӵ�Ũ�ȣ�ˮ�ĵ�������ǿ��
������һ�������Ϊ��Դ���KI��Һ��ȡKIO3��ʯīΪ�缫���ϣ�ʱ��������������I���ŵ磬��缫��ӦʽΪI-+3H2O-6e-=IO3-+6H+���ɹ�ϵʽ��
2Al ---- 6OH-
2��27g 6mol
m/50% 0.5L��0.3 mol��L��1���m=2.7g
��3�������Ȼ����ڼ���������������������ж��Ȼ���Ϊ���ۻ������Ҹ�ԭ�Ӻ���Ϊ8�����ȶ��ṹ������ṹʽΪ��
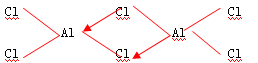
�ڼ��������£���������������̼��Ӧ�����Ȼ�����һ����̼����Ӧ����ʽΪ��
Al2O3+3C+3Cl2 =2AlCl3+3CO.
���㣺�˽�ԭ��صĹ���ԭ������д���缫��Ӧ�͵�ط�Ӧ����ʽ���˽�������ǽ�����Ԫ�����ڱ��е�λ�ü��䵥�ʡ�����������ʺ�Ӧ�á�
���������⿼������������ڱ��е�λ�á����ʺ�Ӧ�ã��绯ѧ��Ӧԭ������ѧ����ʽ����д���ر��ڵڣ�3���⿼�����Ȼ������ӽṹ��ʹѧ����ʶ�������Ǻ�����Ԫ�صĻ����ﶼ�����ӻ�������Ȼ���Ϊ���ۻ�����������۷е�ϵͣ������������ṹ�������ʡ�
�����Ѷȣ�����
2��ѡ���� ��ͼ��ʾ���ձ���ʢˮ����Ȧ����Ȧֱ�������ӣ��ڽ�ͷ����һ����Եϸ�ߵ�סʹ֮ƽ�⣬С�ĵ����ձ��������CuSO4��Һ��һ��ʱ���ɹ۲쵽�������ǣ�������
A����Ȧ�Ա���ƽ��
B����Ȧ������б
C����Ȧ������б
D�������ݲ�������Ȧҡ�ڲ���
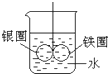
�ο��𰸣���Ȧ����Ȧ���ӽ�������ͭ��Һ�У���װ�ù�����ԭ��أ��ϻ��õ�
���������
�����Ѷȣ���
3��ѡ���� Ǧ����Ч�ʵͣ���Ⱦ��Ŀǰ����п���ȡ��.п��ص�ԭ��Ϊп�������͵������Һ����ط�ӦΪ2Zn+O2=2ZnO�����й���п��ص������У���ȷ����
A��пΪ�������������븺��������Ӧ
B����������������Ӧ������������ԭ��Ӧ
C�������缫��Ӧ�ǣ�Zn �C 2e- +2OH-=ZnO+H2O
D����ع���ʱ����Һ��pH��С
�ο��𰸣�C
���������A����������������Ӧ��ΪZn��Zn�C 2e- +2OH-=ZnO+H2O������������������ԭ��ӦO2+2H2O+4e-=4OH-��B��������������������Ũ�Ȳ��䣬pH���䡣
�����Ѷȣ�һ��
4��ѡ���� �״�ȼ�ϵ�أ�DMFC�������ڱʼDZ����ԡ������ȣ���ȼ�ϵ�����Լ״�Ϊȼ�ϣ�����Ϊ������������ʿ��������ӽ���Ĥ���ɴ��������ӣ���Ҳ�����ǹ���������ɴ��������ӣ����״��������ֱ��ڶ�����缫�Ϸ�����Ӧ���Ӷ�����ѧ��ֱ��ת��Ϊ���ܡ�
�������������� [???? ]
A����طŵ�ʱ���״��ڸ�������������Ӧ
B���Թ���������Ϊ����ʵĵ�طŵ�ʱ���������ɸ�����������
C�������ӽ���ĤΪ����ʵĵ�طŵ�ʱ�������ķ�ӦΪ��O2+4H++4e-==2H2O
D����ص��ܷ�Ӧ�ǣ�2CH3OH+3O2==2CO2+4H2O
�ο��𰸣�B
���������
�����Ѷȣ�һ��
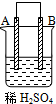
5��ѡ���� ��A��B��C��D���ֽ���������װ�ý���ʵ�飬������������ȷ���ǣ�������
ʵ��װ��������
|
װ��
��
��
��

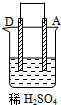
����
���۽���A�����ܽ�
C����������
A�����������
A��װ�ü��е�B������ԭ��صĸ���
B��װ�����е�C������ԭ��ص�����
C��װ�ñ��е�D������ԭ��ص�����
D�����ֽ����Ļ�����˳����D��A��B��C
�ο��𰸣�A��ԭ����и�������ʧ���ӣ������������ᣬ����A�Ǹ�������A
���������
�����Ѷȣ���
|