微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中,正确的是:
A.钢铁腐蚀的负极反应为:Fe-3e- = Fe3+
B.Mg―Al及NaOH溶液构成的原电池中负极材料为Mg
C.甲烷燃料电池的正极反应为:O2+2H2O+4e-=4OH-
D.乙醇燃料电池的电解质常用KOH,该电池的负极反应为:
C2H5OH-12e-=2CO2↑+3H2O
2、选择题 有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3。电池的总反应式为:2H2+O2===2H2O,负极反应为H2+CO-2e-===H2O+CO2。该电池放电时,下列说法中正确的是( )
A.正极反应为2H2O+O2+4e-===4OH-
B.常温常压下每消耗22.4LH2向外电路提供的电子小于2mol
C.电子由正极经外电路流向负极
D.电池中CO的物质的量将逐渐减少
3、填空题 甲醇是重要的化工原料,在日常生活中有着广泛的应用。 ??
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g)+2H2?(g)?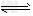 CH3OH(g)?????△H1
CH3OH(g)?????△H1
反应Ⅱ:CO2(g)+3H2?(g) ?CH3OH(g)+H2O(g)??△H2
?CH3OH(g)+H2O(g)??△H2
在以上制备甲醇的两个反应中,反应I优于反应Ⅱ,原因为____________
下表所列数据是反应I在不同温度下的化学平衡常数的数值:??

①在一密闭容器中发生反应工并达到平衡后,保持其他条件不变,对容器升温,此反应的化学平衡应____(填“正向”“逆向”或“不”)移动。
②某温度下,将1?mol?CO和4mol?H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.1?mol/L,则CO的转化率为____,此时的温度____(填“>”“<”或 “=”)250℃。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+ 4H2O(l)??△H1=-Q1?kJ/mol
②2CO(g)+O2(g)=2CO2(g)????△H2=-Q2?kJ/mol
③H2O(g)=H2O(l)???△H3=-Q3?kJ/mol
请写出甲醇发生不完全燃烧生成一氧化碳和气态水的热化学反应方程式:_____________。
(3)某同学依据甲醇燃烧的反应原理,设计如图所示的电池装置,工作一段时间后,测得溶液的pH将_____________(填“升高” “降低”或“不变”),该燃料电池负极反应的离子方程式为_____________。

4、选择题 海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4A1+3O2+6H2O=4A1(OH)3,下列说法错误的是(????)
A.该装置能实现化学能转化为电能
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面
D.该电池通常只需更换铝板就可继续使用
5、选择题 高铁电池是电动汽车首选的电池之一,该电池的工作原理为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是 ( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列关于该电池放电时的说法中正确的是 ( )
A.高铁电池产生的电流从负极经外电路到达正极
B.正极反应式为Zn+2OH-―2e - =Zn(OH)2
C.负极pH减小,正极pH增大,电解液pH增大
D.每氧化1mol高铁酸钾转移3mol电子