微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)(1)质量都是50g的HCl、NH3、CO2、O2四种气体中,含分子数最少的是 ;在同温同压下,密度最小的是 (填分子式)。
(2)在 mL0.2 mol/LNaOH溶液中含1g溶质;配制50mL0.2 mol/LCuSO4溶液,需要CuSO4.5H2O g。
(3) 标准状况下,33.6LHCI气体溶于水配成1L溶液,则溶液中溶质的物质的量浓度为 mol/L。
(4)质量分数为49%的硫酸溶液,其密度为1.4g/cm3,则其物质的量浓度为 mol/L。
(5)有一种气体的质量是14.2g,在标准状况下的体积是4.48L,则该气体的摩尔质量为 g/mol。
参考答案:(1)CO2;NH3 &#
本题解析:
试题分析:(1)质量相同时, ,CO2的摩尔质量最大,所以分子数最少。
,CO2的摩尔质量最大,所以分子数最少。 ,NH3的摩尔质量最小,所以密度最小。
,NH3的摩尔质量最小,所以密度最小。
(2)根据n=cV可得V= 。m=0.05L×0.2mol/L×250g/mol=2.5g。
。m=0.05L×0.2mol/L×250g/mol=2.5g。
(3)c= 。
。
(4)c= 。
。
(5)M=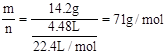 。
。
考点:物质的量计算
点评:本题非常基础简单,主要考查物质的量的基本公式计算。
本题难度:一般
2、选择题 设nA 为阿伏加德罗常数的数值 ,下列说法正确的是(相对原子质量:O-16)
A.常温下,8gO2和O3的混合气体中含有4nA个电子
B.1molFe2+与足量的H2O2溶液反应,转移2nA个电子
C.1 L 0.1 mol ・L-1NaHCO3液含有0.1nA个HCO3-
D.常温常压下,22.4L的NO2 和C O2混合气体含有2 nA个氧原子
参考答案:A
本题解析:
试题分析:氧气和臭氧互为同素异形体,氧元素的质量分数都是100%,则混合气体中氧元素的质量分数都是100%,则混合气体中氧原子的质量为8g,由于n=m/M,则氧原子的物质的量为0.5mol,氧原子的电子数等于质子数,1mol氧原子含有8mol电子,0.5mol氧原子含有4mol电子,故A项正确;双氧水将亚铁离子氧化为铁离子,铁元素的化合价由+2升为+3价,化合价升高1,则2Fe2++H2O2+2H+=2Fe3++2H2O~2e-,该反应中亚铁离子与转移电子的系数之比等于物质的量之比,则2mol亚铁
本题难度:一般
3、选择题 下列叙述正确的是??(????)
A.1 mol  H2SO4的质量为98 g・mol-1
H2SO4的质量为98 g・mol-1
B.H2SO4的摩尔质量为98 g
C.98 g H2SO4含有NA个H2SO4分子
D.6.02×1023个H2SO4分子的质量为9.8 g
参考答案:C
本题解析:略
本题难度:简单
4、简答题 将甲烷和氧气按一定物质的量之比混合点燃后,测得生成物总质量为18.4g,将全部生成物通过足量浓硫酸后,质量减少了9g.
(1)通过计算可得出原混合气体中甲烷的物质的量为______mol.
(2)通过对(1)计算结果的进一步分析,可推知原混合气体反应后的生成物应为______和水组成的混合物(填化学式).
(3)求原混合气体中甲烷和氧气的物质的量之比(写出详细的计算过程).
参考答案:(1)将全部生成物通过足量浓硫酸后,质量减少了9g,则应为水
本题解析:
本题难度:一般
5、选择题 某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏低。该学生得出了以下原因,其中是使溶液浓度偏低的原因的是
A.容量瓶刚用氢氧化钠溶液润洗过
B.在转移溶液时不小心洒落瓶外
C.在烧杯中溶解了氢氧化钠后,趁热将溶液到入容量瓶,并迅速配成了溶液
D.定容时,俯视刻度线
参考答案:B
本题解析:A 相当于溶质放的多,所配溶液浓度偏高
B 相当于溶质有损失,所配溶液浓度偏低
C 冷却后溶液体积会变小,趁热定容,相当于溶剂放的少,所配溶液浓度偏高
D定容时,俯视刻度线,溶剂放的少,所配溶液浓度偏高。故选B 。
本题难度:简单