微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 (14分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。

(1)B中反应的离子方程式是____。
(2)A中溶液变红的原因是____。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在?????。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是SCN―与Cl2发生了反应。
(4)甲同学猜想SCN―可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN―的电子式为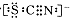
①甲同学认为SCN―中碳元素没有被氧化,理由是?????????。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN―中被氧化的元素是??????????。
③通过实验证明了SCN―中氮元素转化为NO3-,他的实验方案是____。
④若SCN―与Cl2反应生成1 mol CO2,则转移电子的物质的量是??????mol。
参考答案:(14分)
(1)Cl2+2 OH-= Cl-+ Cl
本题解析:
试题分析:(1)B中是氯气与氢氧化钠的反应,离子方程式为Cl2+2 OH-= Cl-+ ClO-+ H2O;
(2)A中的Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色Fe(SCN)3,所以溶液变红
(3)①加入NaOH溶液,有红褐色沉淀生成,此红褐色沉淀为氢氧化铁沉淀,则溶液中一定存在Fe3+
(4)①因为SCN―中碳元素已经是最高价态+4价;
②与盐酸酸化的BaCl2溶液,产生白色沉淀,此白色沉淀为硫酸钡沉淀,所以被氧化的元素是硫元素;
③证明S
本题难度:一般
2、填空题 (12分)已知LiH、NaH及LiAlH4?都是常见的金属的氢化物,其中LiAlH4可由下列途径合成:?4LiH + AlCl3 ? ?LiAlH4+ 3LiCl。
?LiAlH4+ 3LiCl。
试探究下列相关问题
(1)下列有关说法正确的是???????????▲??????????。
A.该反应是氧化还原反应
B.乙醚(C2H5OC2H5)是非极性分子
C.化学性质锂与镁相似,铝与铍相似
D.LiAlH4具有还原性
(2)正在载入...
镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力,其中铜钙合金的晶胞结构为:
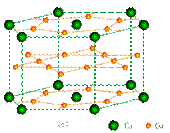
试回答下列问题
①在周期表中Ca处于周期表????▲?????区。
②铜原子的基态核外电子排布式为:??????????????????????????????????▲????????????????????????。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm3,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n= ????▲???(填数值);氢在合金中的密度为:???▲???。
(3)中美科学家合作发现钙和锶在C60上吸附很强,可以均匀地覆盖在C60表面上,形成M32C60。非常适于实际应用。 Ca32C60上可吸附至少92个氢分子(如图)。

有关说法正确的是?????????????▲??????????。
A.钙的第一电离能和电负性均比锶的第一电离能小
B.C60中碳原子杂化方式为sp3
C.Ca32C60储氢是与H2发生加成反应
D.吸附相同数目氢分子时,储氢质量分数(wt%。)Ca32C60比Sr32C60高
参考答案:(1)BCD
(2)①S ?②[Ar]3d104s1
本题解析:略
本题难度:简单
3、选择题 下列铁的合金中,含碳量最高的是
A.生铁
B.高碳钢
C.低碳钢
D.不锈钢
参考答案:A
本题解析:
本题难度:简单
4、填空题 (13分)已知某工业废水中含有大量FeSO4,较多的Cu2+,少量的Na+ 以及部分污泥,通过下列流程可从该废水中回收FeSO4・7H2O晶体及金属Cu。
Y溶液
?
 (1)步骤 (1)步骤 1的主要操作是????????,需用到的玻璃仪器有???????, _______、????????。 1的主要操作是????????,需用到的玻璃仪器有???????, _______、????????。
(2)步骤2中发生反应的离子方程式为???????????????????????????????
(3)步骤3中加入的Y溶液是????????????(填化学式)
(4)步骤4中涉及的操作是:蒸发浓缩.?????????????.过滤.洗涤.烘干。
(5)实验室要配制100mL1.0mol・L-1 FeSO4溶液,经计算,应该用托盘天平称取FeSO4・7H2O固体????????g。
参考答案: 本题解析:略 本题解析:略
本题难度:困难
5、选择题 下列金属冶炼的反应原理,错误的是(???)
A.2NaCl(熔融) 2Na+Cl2? 2Na+Cl2?
B.MgO+H2 Mg+H2O Mg+H2O
C.Fe3O4+4CO  3Fe+4CO2 3Fe+4CO2
D.2HgO  2Hg+O2? 2Hg+O2?
参考答案:B
本题解析:钠、镁等活泼的金属,要通过电解法进行冶炼,所以A正确,B不正确。不活泼的金属通过热分解即可,D正确。介于中间的金属,一般通过还原剂还原进行冶炼,C正确。答案选B。
本题难度:简单
|