微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)将一小块金属钠投入盛有水的烧杯中,发生反应的化学方程式为??????????:
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是??????(填化学式,下同);适宜做耐火材料的是??????;
(3)金属铝既能与盐酸反应,又能与烧碱溶液反应,请写出金属铝与烧碱溶液反应的离子方程式:??????????。
(4)取少量FeCl2溶液,按图所示操作,使其跟NaOH溶液反应。?可观察到试管中出现白色絮状沉淀,继而变成灰绿色,最后变成红褐色,请写出与上述现象相关的反应的化学方程式:???????????、????????????。
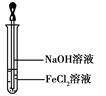
(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是???(填序号)。
A.有铜无铁
B.有铁无铜
C.铁、铜都有
D.铁、铜都无
参考答案:(1)2 Na + 2 H2O =2 NaOH + H2↑;
本题解析:
试题分析:(1)钠与水反应生成氢氧化钠和氢气,化学方程式为2 Na + 2 H2O =2 NaOH + H2↑;
(2)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是Na2O2,适宜做耐火材料的是Al2O3,铁的氧化物适宜做颜料;
(3)金属铝与烧碱溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+H2O ==2AlO2-+H2O;
(4)氢氧化钠与氯化亚铁溶液反应先生成白色沉淀,迅速变成灰绿色,最终成为红褐色,发生的化学方程式为FeCl2 + 2NaOH =
本题难度:一般
2、计算题 (10分)将一定质量的Al、Fe混合物加入到足量的盐酸中,充分反应后得到标准状况下的氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气6.72L。
⑴.写出与碱反应涉及的化学方程式:_____________________________
⑵.混合物中Al和Fe的质量分别为________和__________
⑶.当混合物与盐酸反应时,转移电子数为_______mol;与NaOH溶液反应时转移电子数为_______mol。
参考答案:(10分)
⑴.2Al+2NaOH+2H2O=2NaA
本题解析:略
本题难度:简单
3、填空题 铁黄是一种重要的颜料,化学式为Fe2O3・xH2 O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含FeZ 0。及少量的CaO, Mg0等)和黄铁矿粉
(主要成分为FeS2)制备铁黄的流程如下:
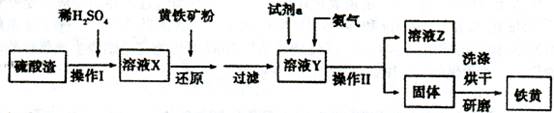
(1)操作I与操作II中都用到玻璃棒,玻璃棒在两种操作中的作用分别是_?????、??????
(2)试剂a最好选用_???(供选择使用的有:铝粉、空气、浓HNO3 );其作用是_???????????。
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是_???????_(填序号)。
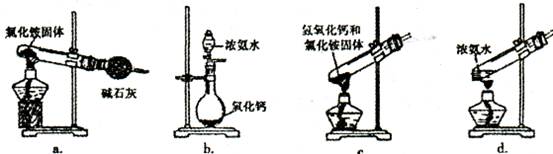
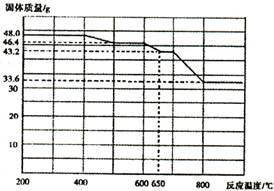
(4)查阅资料知,在不同温度下Fe2 O3被CO还原,产物可能为Fe3 O4?、FeO或Fe,固体质量与反应温度的关系如右图所示。根据图象推断670℃时Fe2 O3还原产物的化学式为M,并设计一个简单的实验,证明该还原产物的成分(依次填写每步操作中所加试剂的化学式、现象和结论)。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2 O2溶液 、NaOH溶液、KSCN溶液。
加入试剂
| 现象
| 结论
|
?
| ?
| 则还原产物为?????
|
?
| ?
|
?
| ?
?
参考答案:
(1)搅拌加速溶液;引流。(2)空气;作氧化剂,将二
本题解析:
试题分析:(1)操作I是搅拌加速溶液溶解,操作II是过滤操作,主要用到玻璃棒引流。(2)试剂a最好选用空气,来源廉价,其作用是作氧化剂,将二价铁离子氧化为三价铁离子。(3)实验室制氨气的主要是操作简单,制作方便,由于氨气易溶于水,故要加热,可选择bd。(4)对于二价铁离子有无可用KSCN溶液不显红色判断,对于有无固体铁可用加入酸有无气泡做出判断。CO还原氧化铁的还原产物为可能Fe3O4,FeO和Fe,Fe2O3加热温度可达到500℃~600℃,质量由46.4g减少为45g,还原产物为Fe3O4;6
本题难度:困难
4、选择题 类推的思维方法在化学学习和研究中经常用到,但是有时会产生错误的结论。因此,推出的结论最终要经过检验才能决定其是否正确。以下几种类推结论不正确的是
A.金属镁失火不能用CO2灭火器灭火;金属钠失火也不能用CO2灭火器灭火
B.Fe3O4可以写成FeO・Fe2O3;Pb3O4也可以写成PbO・Pb2O3
C.不能用电解AlCl3溶液来制取金属铝;也不能用电解MgCl2溶液来制取金属镁
D.Al和S直接化合时可得到Al2S3;Fe与S直接化合时也可得到Fe2S3
参考答案:BD
本题解析:A中因Mg在CO2中能继续燃烧,不能用CO2来扑灭;而Na因燃烧后生成的Na2O2会和CO2发生反应:2Na2O2+2CO2====2Na2CO3+O2,有O2生成,从而达不到灭火的目的。B中Fe3O4,因铁显+2、+3价,故可写成FeO・Fe2O3的形式;但Pb3O4中的Pb分别显+2、+4价,所以可写成2PbO・PbO2,但不能写成PbO・Pb2O3的形式。C项中,因Mg是比Al更活泼的金属,Al不能用电解AlCl3溶液的方法来制取,Mg也不能用电解MgCl2溶液的方法制取。D中因S的氧化性较弱,不能
本题难度:简单
5、填空题 现有下列四种物质:①NH4Cl、②Cl2、③FeCl3、④NO.其中,能够与氢氧化钙加热条件下反应生成能使湿润的红色石蕊试纸变蓝的气体的是______(填序号,下同),遇到KSCN溶液能变红的是______,易与空气中氧气反应的是______,通常状况下呈黄绿色的是______.
参考答案:NH4Cl与碱反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝;
本题解析:
本题难度:一般
|