微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 250C时,0.1mol・L-1稀醋酸加水稀释,如图中的纵坐标y可以是( )

A.溶液的pH
B.醋酸的电离平衡常数
C.溶液的导电能力
D.醋酸的电离程度
参考答案:C
本题解析:
试题分析:A、醋酸是弱电解质,加水稀释促进电离,氢离子的物质的量增大,溶液的体积也增大,0.1mol・L-1稀醋酸加水稀释,溶液体积增大为主,所以溶液中氢离子浓度逐渐减少,溶液的pH逐渐增大,但始终小于7,错误;B、温度不变,醋酸的电离平衡常数不变,错误;C、醋酸是弱电解质,加水稀释促进电离,氢离子的物质的量增大,溶液的体积也增大,0.1mol・L-1稀醋酸加水稀释,溶液体积增大为主,所以溶液中氢离子、醋酸根浓度逐渐减少,溶液的导电能力逐渐减小,正确;D、加水稀释促进醋酸电离,醋酸的电离程度增大,
本题难度:简单
2、填空题 (8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 Ka= 1.75×10-5
碳酸 Ka1= 4.30×10-7 Ka2 = 5.61×10-11
亚硫酸 Ka1= 1.54×10-2 Ka2 = 1.02×10-7
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = ;
碳酸的第一步电离比第二步电离 (填“容易” 或 “困难”)。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > >
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是 (填序号)
A.c(CH3COO-)
B.c(H+)
C.醋酸的电离平衡常数
D.醋酸的电离度
参考答案:(1) 本题解析:(1)碳酸的第一步电离方程式为H2CO3
本题解析:(1)碳酸的第一步电离方程式为H2CO3 H++HCO3-,所以电离平衡常数表达式为Ka1 =
H++HCO3-,所以电离平衡常数表达式为Ka1 = 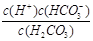 。由于第一步电离出的氢离子会抑制第二步的电离,所以碳酸的第一步电离比第二步电离容易。
。由于第一步电离出的氢离子会抑制第二步的电离,所以碳酸的第一步电离比第二步电离容易。
(2)酸电离平衡常数越大,说明酸越强。所以根据电离平衡常数可知,H2CO3、HCO3-和HSO3-的酸性强弱顺序为H2CO3 > HSO3- > HCO3-。
(3)加入乙酸,增大氢离子浓度,抑制醋酸的电离,所以选项AD减小,B增大,C不变。
本题难度:一般
3、选择题 不能用于判断HA是弱电解质(弱酸)的依据是 [???? ]
A.浓度相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多
B.pH相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多
C.浓度相等的HCl与HA两溶液,C(HCl中H+)约是C(HA中H+)的100倍
D.pH相等的HCl与HA两溶液,C(HA)约是C(HCl)的100倍
参考答案:A
本题解析:
本题难度:一般
4、选择题 已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH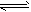 CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中
c(H+)/c(CH3COOH)值增大,可以采取的措施是
[???? ]
A.加少量烧碱溶液
B.降低温度
C.加少量冰醋酸
D.加水
参考答案:D
本题解析:
本题难度:一般
5、填空题 分I:化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一。(1)化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是
A.定性检验SO32-,可用HNO3酸化的BaCl2溶液
B.配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度
C.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液
D.酸性高锰酸钾溶液经常用盐酸酸化
(2)下列有关说法中正确的有?????????
①用pH试纸测得氯水的pH为3.5
②用瓷坩埚高温熔融NaOH固体
③加入浓NaOH溶液,加热产生使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定含有NH4+
④向溶液中加入少量双氧水,再加几滴KSCN溶液后溶液变红,则原溶液中一定含有Fe2+
⑤实验时不慎被玻璃划破手指,引起轻微流血时,可用三氯化铁溶液涂抹止血
II:(1)某温度下,纯水中c(H+)=2.0×10-7mol・L-1.该温度下,0.9mol・L-1NaOH溶液与0.1mol・L-1 HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH= ??????。
(2)向含有0.020 molCH3COOH的溶液中加入0.020mol CH3COONa固体,溶液pH增大,主要原因是??????;已知该混合溶液中c(Na+)<c(CH3COO-),则c(CH3COOH)??????c(CH3COO-)(用“>”、“<”、“=”符号填空)。
(3)常温下,向100 mL 0.01mol・L-1HA溶液逐滴加入0.02mol・L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。

回答下列问题:
①由图中信息可知HA为???酸(填“强”或“弱”)。
②K点对应的溶液中,c(M+)+c(MOH)=?????mol・L-1。
参考答案:Ⅰ(1)C?(2)③⑤???Ⅱ (1)13????(2) C
本题解析:
试题分析:Ⅰ:(1)定性检验SO32-,用HNO3酸化会将其氧化成SO42-, HNO3能将FeCl2氧化为FeCl3,酸性高锰酸钾具有强氧化性,会将盐酸氧化为氯气。(2)pH试纸测得的数值为整数,瓷坩埚中含二氧化硅,会与NaOH,检验有Fe2+需先加KSCN,排除Fe3+的干扰。
本题难度:一般