微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 在如图所示的实验装置中,当A、B、C分别为以下不同组合时,回答有关问题。
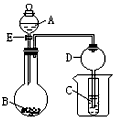
(1)当A为盐酸、B为贝壳(粉末)、C为水玻璃时,小试管中的现象是________________,其中发生的离子反应方程式是________________。
(2)当A为浓氨水、B为生石灰、C为AlCl3溶液,小试管中出现的现象是________________,反应的离子方程式为________________。
(3)当A为浓硫酸、B为Mg、Al、Fe、Cu中的一种银白色片状金属、C为品红溶液,小试管中溶液红色褪去,则B为 (填元素符号), A和B反应的方程式是________________。
(4)装置D的作用是________________。
参考答案:(1)白色胶状物质;SiO32-+CO2+H2O==H2Si
本题解析:
本题难度:一般
2、填空题 醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
①NaBr+H2SO4==HBr+NaHSO4
②R-OH+HBr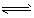 R-Br+H2O
R-Br+H2O
可能存在的副反应有:醇在浓硫酸存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下:

请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是____(填字母,单选)。
a.圆底烧瓶
b.量筒
c.锥形瓶
d.漏斗
(2)溴代烃的水溶性____(填“大于”、“等于”或“小于”)醇的水溶性;其原因是_________ 。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在____(填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的是____(填字母,多选)。
a.减少副产物烯和醚的生成
b.减少Br2的生成
c.减少HBr的挥发
d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是____(填字母,单选)。
a.NaI
b.NaOH
c.NaHSO3
d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,有利于___________ ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是___________。
参考答案:(1)d
(2)小于; 醇分子可与水分子形成氢键,溴
本题解析:
本题难度:一般
3、推断题 三氯化铁是中学化学实验室中必不可少的重要试剂。某同学利用废铁屑(含少量铜等不与盐酸反应的杂质)来制备FeCl3・6H2O,该同学设计的实验装置如图所示,A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,从分液漏斗内向A中加过量的盐酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3・6H2O晶体。填写下列空白

(1)收集B处的气体可采用的方法是________________________。
(2)滴加盐酸时,发现反应速率较盐酸与纯铁粉反应的要快,其原因是________________________。
(3)烧杯内盛放过量稀HNO3的原因是___________________,反应的离子方程式是_________________。
(4)整个实验过程中,旋塞a都必须打开,除了为排出产生的气体外,另一个目的是___________________________________。
(5)将烧杯内溶液用蒸发、浓缩、再降温结晶法制得FeCl3・6H2O,而不用直接蒸干的方法来制得晶体的理由是______________________。
参考答案:(1)排水集气法或向下排空气法
(2)废铁屑中有Cu
本题解析:
本题难度:一般
4、实验题 实验室中以铝土矿(主要成分是Al2O3和少量的SiO2和Fe2O3杂质)为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2・12H2O]的工艺流程如下:
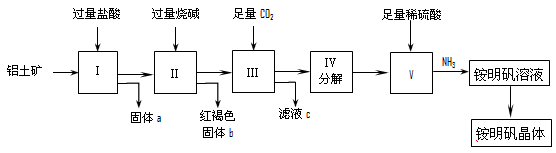
试回答下列问题:
⑴固体a的化学式为_____,III中通入过量CO2气体的离子方程式为____________ 。
⑵由V制取铵明矾溶液的化学方程式为_________________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________ 、冷却结晶、过滤洗涤。
⑶以1000kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3,需消耗质量分数98%的硫酸(密度1.84g/cm3)___________L(保留一位小数)。
⑷若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中Al2O3和H2SO4的物质的量之比为___________。
参考答案:⑴SiO2? ; AlO2-+CO2+2H2O ==HCO3
本题解析:
本题难度:一般
5、选择题 用含有少量镁的铝片制取纯净的Al(OH)3,可能有的步骤为:① 加盐酸溶解;② 加苛性钠溶液;③ 过滤;④ 通入过量CO2;⑤ 加过量纯碱溶液,实验操作最合理的组合及顺序是[???? ]
A.①⑤④③
B.②③④③
C.②③⑤③
D.①⑤③
参考答案:B
本题解析:
本题难度:一般