微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+、Al3+、Cl-、SO42―
B.含有0.1 mol・L-1Fe3+的溶液中:K+、Mg2+、I-、NO3―
C.含有0.1 mol・L-1Ca2+的溶液中:Na+、K+、CO32―、Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、NO3―、SO42―
参考答案:D
本题解析:
试卷分析:强碱性溶液Al3+不能大量共存,含有Fe3+的溶液 I-不能大量共存,含有Ca2+的溶液CO32-不能大量共存。答案选D。
考点:离子共存
点评:离子不能大量共存的一般情况是:(1)能发生复分解反应的离子之间(即生成沉淀,气体,水、弱酸、弱碱等难电离物质);(2)能生成难溶物的离子之间(如:Ca2+和 SO42-;Ag+和 SO42-);(3)能完全水解的离子之间,如多元弱酸和弱碱盐的阴、阳离子(如:Al3+, Fe3+与 CO32-、HCO3-、AlO2-、ClO-,S2-等);(4)能发生氧化还原反应的离子之间(如:Fe 、H+、NO3-;S2-、ClO-;S2-、 Fe3+等);(5)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。
本题难度:困难
2、选择题 有甲、乙、丙三种溶液,进行如下操作:

则甲、乙、丙三种溶液可能是
A.BaCl2、H2SO4、MgCl2
B.CaCl2、HNO3、BaCl2
C.CaCl2、HNO3、NaCl
D.BaCl2、HCl、Na2SO4
参考答案:D
本题解析:
试题分析:碳酸钠溶液与甲反应生成白色沉淀,则甲是氯化钡或氯化钙,白色沉淀是碳酸钡或碳酸钙沉淀。白色沉淀能和过量的乙反应生成气体,因此乙应该是酸。所得溶液中继续加入丙又产生白色沉淀,所以丙应该是硫酸,产生的白色沉淀是硫酸钡,则甲是氯化钡,因此正确的答案选D。
本题难度:一般
3、填空题 (14分)(Ⅰ)A、B、C三种无色可溶性盐分别是由Na+、Ag+ 、Ba2+、Cl―、NO3― 、CO32―中不同的阴、阳离子所组成。经实验A溶液、B溶液均可以与盐酸反应,其中A产生白色沉淀,B产生气泡。则A为??????????、B为????????????。将B和C的溶液混合反应的化学方程式为:??????????????????????????????????????????????????。
(Ⅱ)有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验:
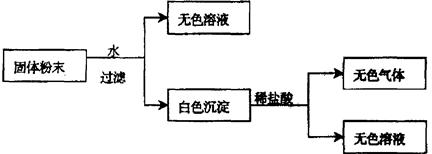
从实验可以判断,该固体粉末中一定不含有????????????????????,
它的组成可能是????????????????????????或???????????????????????????。
参考答案:(14分)(Ⅰ) AgNO3??????Na2CO3????
本题解析:
试题分析:(Ⅰ)B溶液产生气泡,所以B中含有CO32-,所以B是碳酸钠;A溶液产生白色沉淀,所以A中含有银离子,则A应该是硝酸银,所以C是氧化钡。则B和C反应的方程式是BaCl2+Na2CO3=BaCO3 ↓+2NaCl。
(Ⅱ)固体溶于水是无色溶液和白色沉淀,所以一定没有硫酸铜;由于白色沉淀能溶于盐酸中生成无色气体和无色溶液,所以白色沉淀不是硫酸钡,而是碳酸钙,而硫酸钠和氯化钡不能同时存在,由于该物质是由三种物质组成的,是由其起组成可能是CaCO3、Na2SO4、KNO3 、CaCO3、K
本题难度:一般
4、选择题 下列各组离子能大量共存的是
A.H+、Na+、HCO3-、Cl-
B.Fe3+、SCN-、Cl-、NO3-
C.Mg2+、Fe2+、SO42-、NO3-
D.Fe3+、SO42-、OH-、NO3-
参考答案:C
本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A中H+和HCO3-不能大量共存;B中Fe3+和SCN-不能大量共存;D中Fe3+和OH-不能大量共存,所以答案选C。
本题难度:困难
5、选择题 向下列溶液中分别加入AgNO3溶液和稀HNO3,能生成不溶于稀HNO3的白色沉淀的是
A?.氯水??????????B.氯酸钾????????? C.氯化钾?????????? D.四氯化碳
参考答案:AC
本题解析:
试题分析:氯水和氯化钾能和硝酸银溶液反应生成不溶于稀HNO3的白色沉淀,氯酸钾和四氯化碳中不能电离出氯离子,和硝酸银溶液不反应,答案选AC。
点评:该题是基础性试题的考查,侧重对基础知识的检验。该题的关键是熟练记住常见离子的检验原理、操作要点以及实验现象,然后灵活运用即可。
本题难度:一般