��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ͼ�ס����ǵ绯ѧʵ��װ�á�

��1�����ס������ձ��о�ʢ��NaCl��Һ����
�ټ���ʯī���ϵĵ缫��ӦʽΪ???????��
�������ܷ�Ӧ�����ӷ���ʽΪ????????��
�۽�ʪ��ĵ���KI��ֽ�������ձ��Ϸ���������ֽ�ȱ�������ɫ��������Ϊ������Cl2���������ɵ�I2 ������Ӧ��Cl2��I2�����ʵ���֮��Ϊ5��1���� ���������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ????????��
��2�����������ձ��о�ʢ������CuSO4��Һ����
�ټ��������ϵĵ缫��ӦʽΪ???????��
�������ʼʱ����ʢ��200mLpH=5��CuSO4��Һ(25��)��һ��ʱ�����Һ��pH��Ϊ1����Ҫʹ��Һ�ָ������ǰ��״̬��������Һ�м����������????(д��ѧʽ)��������Ϊ??????????g��????
�ο��𰸣���1����2H2O+O2+4e-===4OH-��
��2C
���������
�������������1���ټ�Ϊԭ���װ�ã�ʯī���������õ��ӷ�����ԭ��Ӧ����ӦΪ2H2O+O2+4e-�T4OH-��
����Ϊ���װ�ã��ɵ��������֪ʯīΪ�����������������ӷŵ磬�����������ӷŵ磬���ⷴӦΪ2Cl-+2H2O H2��+Cl2��+2OH-��
H2��+Cl2��+2OH-��
��Cl2���������ɵ�I2��ClԪ�صĻ��ϼ۽�
�����Ѷȣ�һ��
2��ѡ���� ����һ���ƶƼ���Ϊ��ֹ�����⣬������������һ��ͭ�������������յĵ��ԭ��������ΪͭƬӦ������������
A������
B������
C������
D������
�ο��𰸣����ݵ��ԭ������Cu��FeƬ�϶�ͭʱ���Ƽ���Ϊ�������Ʋ����
���������
�����Ѷȣ�һ��
3��ѡ���� ��ʯī�缫���100 mL����ͭ������Ļ����Һ��ͨ��һ��ʱ����������ռ���2.24 L���壨��״������ԭ�����Һ��Cu2+�����ʵ���Ũ�ȣ�mol��L��1��Ϊ
A��4
B��3
C��2
D��1
�ο��𰸣�D
����������������ͭ������Ļ����Һ�������缫��ӦʽΪ��4OH����4e��=O2+2H2O��
�����缫��ӦʽΪ��2Cu2++4e��=2Cu����Cu2+ȫ���ŵ���Ϻ���Һ�е�H+�����ŵ磬�缫��ӦʽΪ��2 H++2 e��=H2������������ԭ��Ӧ�����е�ʧ��������ȵأ������ԭ�����Һ��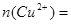 0.1 mol�����ɵ�ԭ�����Һ
0.1 mol�����ɵ�ԭ�����Һ
�����Ѷȣ�һ��
4������� X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�ء�
��֪���� X�ɷֱ���Y��W�γ�X2Y��X2Y2��XW�ȹ��ۻ������ Z�ɷֱ���Y��W�γ�Z2Y��Z2Y2��ZW�����ӻ����??
��ش�
��1��Z2Y�Ļ�ѧʽ��???????????????��??
��2��Z2Y2��X2Y��Ӧ�Ļ�ѧ����ʽ��????��
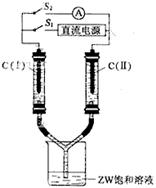
��3����ͼ��ʾװ�ã�����������ʢ�����з�̪��Һ��ZW������Һ��C����C����Ϊ���ʯī�缫��
��ͨS1��C��������Һ��죬�������������������ɡ�??һ��ʱ�������������Һ��δ����缫�����Ͽ�S1����ͨS2����������ָ�뷢��ƫת����ʱ��
C��I���ĵ缫������???????????����д����������
C��II���ĵ缫��Ӧʽ��?????????????????????????��
��4��ͭм����ϡ���������Ӧ������ϡ�����м���X2Y2��ͭм�����ܽ⣬�÷�Ӧ�����ӷ���ʽ��????????????????????��
�ο��𰸣���1��Na2O?? (2)2Na2O2+2H2O��4NaOH
���������
�����������ѧ��A2B2�͵Ļ�������ҪָNa2O2�� H2O2�����ۻ�������H2O2�����ӻ�������Na2O2�����Ը���X��Y��Z��W��ԭ��������С˳����ж�X��H��Y��O��Z��N a��W��Cl��
��1��Z2Y�Ļ�ѧʽ��Na2O��??
��2��Z2Y2��X2Y��Ӧ�Ļ�ѧ����ʽ��2Na2O2+2H2O��4NaOH+O2����
��3������װ��ͼ��֪����ͨS1���װ���ǵ��أ����൱���Ƕ��Ե缫��ⱥ���Ȼ�����Һ��C��������Һ��죬˵���õ缫�����������ɵ�����������������һ�缫���ɵ�����
�����Ѷȣ�һ��
5��ѡ���� �����������������IJ�����ߣ��Ͼɵ�ر�����м��д��������ⱻ�ᵽ�������������ճ̣�����Ҫԭ���ǣ�������
A�����շϾɵ�ص�ʯī�缫����
B�����շϾɵ����ǵĽ�������
C����ֹ�Ͼɵ������©�ĵ���ʸ�ʴ������Ʒ
D����ֹ����й����Ӻ�Ǧ���ؽ���Ԫ�ض�������ˮԴ����Ⱦ
�ο��𰸣�D
���������
�����Ѷȣ���