微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将H2、N2、O2三种气体分别放入不同容器中,使它们的温度、密度相同,则其压强(p)大小的关系,符合
A.p(H2)>p(O2)>p(N2)
B.p(O2)>P(N2)>p(H2)
C.p(H2)>P(N2)>p(O2)
D.P(N2)>p(O2)>p(H2)
参考答案:B
本题解析:由PV=nRT,可推出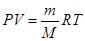 ,
,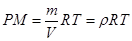 ,也就是当温度、密度相同时,摩尔质量与压强成反应比,则B项符合题意
,也就是当温度、密度相同时,摩尔质量与压强成反应比,则B项符合题意
本题难度:一般
2、选择题 在体积为x L的密闭容器中通入a mol?NO和b mol?O2,反应后容器内氮原子数和氧原子数之比为( )
A.
a
b
B.a
2b
C.a
(a+2b)
D.a
2(a+b)
参考答案:C
本题解析:
本题难度:简单
3、选择题 等质量的SO2和SO3中,下列说法正确的是[???? ]
A.所含氧原子的个数比为2∶3
B.所含硫原子的个数比为1∶1
C.所含氧元素的质量比为5∶6
D.所含硫元素的质量比为5∶4
参考答案:CD
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数,下列叙述中,正确的是
A.常温常压下,5.6 g N2和CO混合物中所含有的原子总数为0.4NA
B.0.1 molNa2 O2中所含的阴离子数为0.2NA
C.将0.2 molFeCl3水解制成胶体,所得胶体粒子数为0.2 NA
D.标准状况下,2.24 L H2O中含有的氧原子数目为0.1 NA
参考答案:A
本题解析:
试题分析:N2和CO 的摩尔质量都是28g/mol,所以5.6g混合物含分子:5.6g÷28g/mol=0.2mol,二者都是双原子分子,所以含有的原子总数为0.4NA,故A项正确;O22?为原子团,为1个离子,所以0.1 molNa2 O2中所含的阴离子数为0.1NA,B项错误;胶体离子为多个分子或原子的集合体,将0.2 molFeCl3水解制成胶体,所得胶体粒子数小于0.2 NA,C项错误;标准状况下水不是气体,所以2.24 L H2O中含有的氧原子数目不是0.1 NA,故D项错误。
本题难度:一般
5、选择题 已知98%的浓硫酸的浓度为18.4mol・L-1,则49%的硫酸溶液物质的量浓度[???? ]
A.等于9.2 mol・L-1
B.大于9.2mol・L-1
C.小于9.2 mol・L-1
D.无法确定
参考答案:C
本题解析:
本题难度:一般
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772
|