微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (17分)
I.(1)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
????Na2SO3+???KIO3+???H2SO4——???Na2SO4+???K2SO4+??? I2+???H2O
①配平上面的氧化还原反应方程式,将计量数填在方框内。
②其中氧化剂是??????,若反应中有5 mol电子转移,则生成的碘是??????mol。
(2)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,乙硼烷燃烧热的热化学方程式为????????????。
II.含氰化物(有CN-)的废水危害大,CN-的含量为0.01mol/L~0.04mol/L就能毒 杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
(1)二氧化钛在上述反应中的作用是??????????????????。
(2)CNO-经进一步处理后产生的两种无毒气体应该是??????????和?????????。
(3)若用NaClO溶液处理NaCN的废液,产生另外两种盐,其化学方程式为?????。
2、选择题 某氧化剂中,起氧化作用的是X2O72-离子,在溶液中0.2mol该离子恰好能使0.6mol的SO32-离子完全氧化,则X2O72-离子还原后X的化合价为
A.+1
B.+2
C.+4
D.+3
3、选择题 2011年4月10日,我国在西昌卫星发射中心用“长征三号甲”运载火箭,成功将第八颗北斗导航卫星送入太空预定转移轨道。该火箭所用燃料是偏二甲肼(CH3-NH-NH-CH3)和四氧化二氮(N2O4)。在火箭升空过程中,燃料发生反应:CH3-NH-NH-CH3+2N2O4→2CO2+3N2+4H2O,提供能量。下列有关叙述正确的是(?)

A.该反应中N2O4是氧化剂,偏二甲肼是还原剂
B.N2是氧化产物,CO2是还原产物
C.CO2是氧化产物,N2是还原产物
D.每有0.6molN2生成,转移电子数目为2.4NA
4、选择题 做实验时不小心使皮肤上粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO+C2O42-+H+→CO2↑+Mn2++  。下列有关叙述正确的是[???? ]
。下列有关叙述正确的是[???? ]
A.发生还原反应的是C2O42-
B.该离子方程式右侧方框内的产物是OH-
C.10 mol H+参加反应时,电子转移5 mol
D.1 mol草酸分子中含有9 mol共用电子对
5、简答题 (1)在-50℃时,液氨存在如下电离:2NH3?NH4++NH-2,k=2×10-12,液氨的电离达到平衡时,各微粒的浓度大小关系为______,加入NH4Cl固体,K______2×10-12(填“<”、“>”或“=”)
(2)已知25℃时Ksp(AgCl)=1.8×10--10,在10mL?0.10mol/L?AgNO3溶液中加入10mL0.20mol/LNaCl溶液,充分反应后溶液中的c(Ag+)=______.
(3)配平硫酸亚铁加强热制备铁红和生成硫的两种常见氧化物的化学方程式:
______FeSO4
高温
______Fe2O3+____________+____________
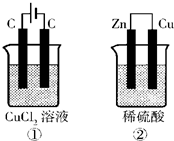
(4)已知氯气能溶于水,溶液呈酸性.如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是______
A.产生气体的体积:①>②
B.溶液的pH变化:①减小,②增大
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极?2Cl--2e-?Cl2↑?? ②中负极?2H++2e-?H2↑