微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2・2H2O)。

(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
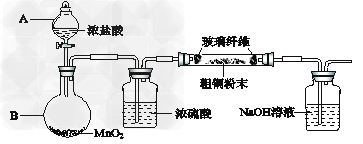
①仪器A的名称是_______________。
②?装置B中发生反应的离子方程是_____________?。
③?有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)____________。
(2)试剂X用于调节pH以除去杂质,?X可选用下列试剂中的(填序号)__________。
a.NaOH???b.NH3・H2O???c.CuO???d.Cu2(OH)?2CO3???e.CuSO4
(3)在溶液2转化为CuCl2・2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+ (aq)?+4Cl-(aq)?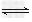 CuCl42-(aq)?+4H2O(l)?
CuCl42-(aq)?+4H2O(l)?
蓝色 黄色
①?上述反应的化学平衡常数表达式是K=?_____________。若增大氯离子浓度,K值(填“增大”、“减小”或“不变”)??????。
②?取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号)_____________。
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
2、实验题 下图是实验室制取乙酸乙酯的装置。
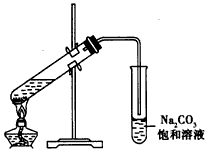
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液的方法:将_____________________,并轻轻地振荡试管,使之混合均匀。
(2)装置中通蒸气的导管要插在饱和Na2CO3溶液的液面上,不能插入溶液中,目的是防止Na2CO3溶液的倒吸,造成倒吸的原因是________________________。
(3)浓硫酸的作用是:①________________________;②________________________。
(4)饱和N2CO3溶液的作用是____________________________。
(5)实验中生成的乙酸乙酯,其密度比水_______(填“大” 或“小”),有_______气味。
(6)若实验中温度过高,使反应温度达到140℃左右时,副反应的主要有机产物有________________(填物质名称)。
3、选择题 用含少量镁的铝片制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是[???? ]
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入过量 CO2生成Al(OH)3沉淀 ⑤加入盐酸生成Al(OH)3沉淀 ⑥加入过量烧碱溶液
A.①⑥⑤③??????????
B.②③⑤③???????????
C.②③④③?????????
D.①③⑤③
4、实验题 “酒是陈的香”的原因之一是储存过程中生成了有香味的酯。实验室用下图所示装置制取乙酸乙酯。
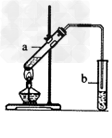
(1)试管a中生成乙酸乙酯的化学反应方程式是???????????????????? 。
(2)试管b中盛放的试剂是????????????????? 溶液,试管b中的导管不伸入液面下的原因是????????????????? 。试管b中发生反应的化学方程式是???????????????????? 。
(3)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有( 填序号)????????????????????? 。
①单位时间里,生成1mol 乙酸乙酯,同时生成1mol 水
②单位时间里,生成1mol 乙酸乙酯,同时生成1mol 乙酸
③单位时间里,消耗1mol 乙醇,同时消耗1mol 乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
5、实验题 MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下:
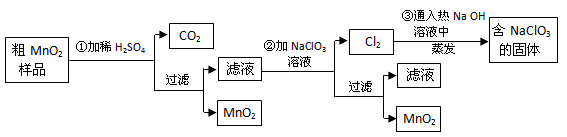
(1)第①步加稀H2SO4时,粗MnO2样品中的__________(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式是:____+ ____ClO3-+ ____= ____MnO2↓+___ Cl2↑+_____ ;反应中氧化剂是___________ 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、______ 、_________ 、玻璃棒。
(4)已知2H2O2(l)=2H2O(l)+O2(g) △H=a kJ・mol-1 反应过程的能量变化如图所示。则
① 该反应为_________ 反应(填“吸热”或“放热”)。
②请用虚线在下图中画出使用MnO2作催化剂的情况下反应过程中体系能量变化示意图。
