微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在实验室制备CH3COOC2H5时在反应试管中不需要添加的试剂是( )
A.C2H5OH
B.CH3COOH
C.浓硫酸
D.碳酸钠溶液
参考答案:D
本题解析:
本题难度:一般
2、实验题
Fe(OH)2是铁的一种氢氧化物,难溶于水,具有还原性,其制备方法较为特殊。下面是实验室制备
Fe(OH)2的方法之一:
(1)制备原理:利用复分解反应,使可溶性的亚铁盐溶液与可溶性的碱液反应生成Fe(OH)2。写出该反应的离子方程式_________________。
(2)NaOH溶液的制备:在试管中加入2~3 mL蒸馏水,加热至沸腾,冷却至室温,加入1片NaOH固体。制备NaOH溶液的蒸馏水加热的目的是___________。
(3)FeSO4溶液的制备:在试管中加入5 mL蒸馏水,并加热,直至蒸馏水沸腾,然后向蒸馏水中滴入几滴稀硫酸;待蒸馏水冷却至室温,加入少量FeSO4晶体,为了防止溶液中的Fe2+被氧化,在溶液中加入少量
____________。加入FeSO4晶体前在蒸馏水中加入稀硫酸的目的是____________。
(4) Fe(OH)2的制备:下图中的胶头滴管中盛有NaOH溶液,试管中是FeSO4溶液。制备Fe(OH)2时正确的操作是___________(填字母序号),操作过程中________(填“能”或“不能”)振荡试管,原因是___________________。
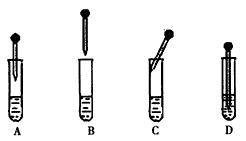
(5)上述方法制备的Fe(OH)2久置也会被氧化,当有1.12 L氧气参与反应时,该氧化过程中转移的电子的物质的量是____。
参考答案:(1)Fe2++2OH-=Fe(OH)2↓
(2)除去
本题解析:
本题难度:一般
3、实验题 实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55~60℃反应。已知苯与硝基苯的基本物理性质如下表所示:

某同学设计如图:
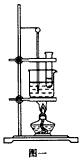
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是____________________________________
(2)分离硝基苯和水的混合物的方法是_____________;分离硝基苯和苯的方法是______________。
(3)某同学用图一装置制取硝基苯:
①用水浴加热的优点是_____________________;
②指出该装置的两处缺陷_____________________;_________________。
参考答案:(1)把浓硫酸缓慢加入浓硝酸中并不断搅拌
(2)分液;
本题解析:
本题难度:一般
4、实验题 聚合硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。现用一定质量的铁的氧化物(如下图)为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+。实验步骤如下:
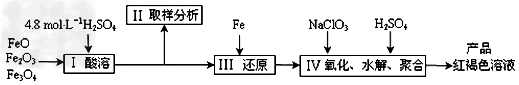
(1)实验室用18.4?mol・L-1的浓硫酸量取_______mL来配制250mL4.8?mol・L-1的硫酸溶液,所用的仪器除烧杯、玻璃棒和移液管外,还需要的玻璃仪器_____________。
(2)步骤II取样分析溶液中的Fe2+、Fe3+的含量,目的是_____________。
A.控制溶液中Fe2+与Fe3+含量比???????
B.确定下一步还原所需铁的量
C.确定氧化Fe2+所需NaClO3的量?????
D.确保铁的氧化物酸溶完全
(3)①写出步骤Ⅳ中用NaClO3氧化时的离子方程式____________________(提示:ClO3-转化为Cl-);
②已知1mol?HNO3的价格为0.16元,1mol?NaClO3的价格为0.45元,评价用HNO3代替NaClO3作为氧化剂的利弊,利是__________,弊是____________。
(4)为了分析产品聚合硫酸铁溶液中SO42-与Fe3+?物质的量之比,有人设计了以下操作
(a)取25mL聚合硫酸铁溶液,加入足量的BaCl2溶液,产生白色沉淀,白色沉淀经过过滤、洗涤、干燥后,称重,其质量为m?g。
(b)另取25mL聚合硫酸铁溶液,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250mL溶液,取该溶液25.00mL,用KMnO4酸性溶液滴定,到达终点时用去0.1000?mol/L?KMnO4标准溶液VmL。离子方程式为:5Fe2+?+?MnO4-+?8H+?=?5Fe3+?+?Mn2+?+?4H2O
①判断(a)步骤溶液中SO42-离子已沉淀完全的方法是__________________;?
②在(b)步骤中判断达到终点的现象是_______________;
③聚合硫酸铁中SO42-与Fe3+的物质的量之比为____________(用含m、V的代数式表示)。
参考答案:(1)65.2mL;250mL容量瓶、胶头滴管
(2)
本题解析:
本题难度:一般
5、实验题 “套管实验”具有装置简洁便利等有优点,结合图示回答有关问题
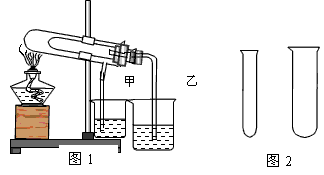
(1)欲利用图1比较碳酸氢钠和碳酸钠的热稳定性,并检验分解产物。最好应在大试管底部加入 _________(填化学式),石灰水变浑浊的烧杯是____________ (填:甲、乙) 。请写出试管中反应的化学反应方程式:____________
(2)使用图2中大小不一的试管,用铝粉和氢氧化钠溶液制取氢气,并收集一试管氢气,将铝粉和氢氧化钠溶液放入___________ 试管内(填:大、小)组成发生装置,请写出该反应的离子方程式为:____________ 为了使得所收集的氢气能较纯净地充满所收集氢气的试管,应如何操作,写出大致的步骤:______________
参考答案:(1)Na2CO3 ;乙 ; 2NaHCO3 == Na2C
本题解析:
本题难度:一般