微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 反应A(g)+B(g) C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
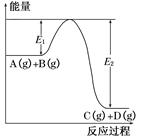
(1)该反应是________(填“吸热”或“放热”)反应。
(2)当反应达到平衡时,升高温度,A的转化率________(填“增大”“减小”或“不变”),原因是________________________________________
(3)反应体系中加入催化剂对反应热是否有影响?________,原因是__________________________________________
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________,E2________。(填“增大”“减小”或“不变”)
参考答案:(1)放热
(2)减小 根据勒・夏特列原理,升高温度有
本题解析:解答第(1)题的关键是读懂图,由图示可知反应物A(g)+B(g)所含的能量大于生成物C(g)+D(g)所含的能量,故该反应为放热反应。解答第(2)题结合第(1)题的推断可知,升高温度平衡向逆反应方向(吸热反应方向)移动,故升高温度,A的转化率减小。第(3)、(4)题,加入催化剂只能改变反应途径,使E1(活化能)减小,E2同时减小,增大反应速率,不改变化学反应的始态和终态的能量,而反应热只与化学反应的始态和终态有关,与反应途径无关,因此使用催化剂对反应热没有影响。
本题难度:一般
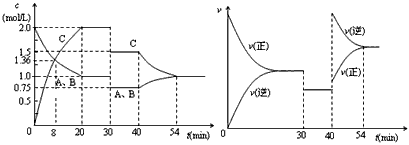
2、选择题 某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应是:A(g)+xB(g)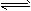 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
 [???? ]
[???? ]
A. 8min前正反应速率大于逆反应速率
B. 20min时A的反应速率为0.05mol/(L・min)
C. 反应方程式中的x=1,正反应为吸热反应
D. 30min时降低温度,40min时升高温度
参考答案:A
本题解析:
本题难度:一般
3、选择题 将CoCl2溶解于盐酸中可以形成[CoCl4]2-,在溶液中存在下面的化学平衡:
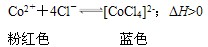
下列说法正确的是
A.该反应的平衡常数K=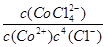
B.升高温度,正反应速率增大,逆反应速率减小
C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小
参考答案:A
本题解析:化学常数是在一定条件下的可逆反应中,当可逆反应反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的方程式可知,选项A正确;升高温度,正逆反应速率都是增大的,选项B不正确;正反应是吸热反应,升高温度,平衡向正反应方向移动,溶液显蓝色,选项C不正确;增大Cl-浓度,平衡向正反应方向移动,Co2+浓度减小,根据勒夏特列原理可知,Cl-浓度是增大的,选项D不正确,答案选A。
本题难度:一般
4、选择题 四个试管中都装有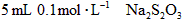 溶液,分别在不同温度下加入硫酸和一定量水,最先出现浑浊的是[???? ]
溶液,分别在不同温度下加入硫酸和一定量水,最先出现浑浊的是[???? ]
A.20℃,10 mL硫酸
B.20℃,5 mL硫酸,5 mL水
C.30℃,5 mL硫酸,2 mL水
D.30℃,4 mL硫酸,3 mL水
参考答案:C
本题解析:
本题难度:一般
5、实验题 已知锌与稀硫酸反应为放热反应,某学生为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
时间(min)
| 1
| 2
| 3
| 4
| 5
|
氢气体积(mL)
| 30
| 120
| 280
| 350
| 370
反应速率最大的(填0~1、1~2、2~3、3~4、4~5min)时间段为 。原因是 。
②反应速率最小的时间段为 ,原因是
(2)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在硫酸溶液中分别加入等体积的下列溶液以减慢反应速率。
A.蒸馏水 B.CuCl2溶液 C.NaCl溶液
你认为他的做法可行的是 (填相应字母);做法不可行的是 (填相应字母),做法不可行的理由是 。
参考答案:(1)①2~3min 该反应是放热反应,此时温度高
本题解析:
试题分析:温度越高,反应速率越快;离子浓度越小,反应速率越慢;增大固体接触面积,反应速率加快,硫酸溶液中加入等体积的NaCl溶液,相当于加水将硫酸稀释,所以氢离子浓度减小,据此可以解答。
(1)①根据表中数据可知,0~1、l~2、2~3、3~4、4~5min各时间段生成氢气的体积分别为30、90、160、70、20,可以看出反应速率最大的是2~3min。这是由于锌与稀硫酸反应为放热反应,随反应的进行,温度越来越高,反应速率加快。
②反应速率最小的时间段为4~5min,这是由于随着反应的进行,氢离子浓度越来越小,反应速率越来越慢。
(2)选项A中在硫酸溶液中加入等体积的蒸馏水,相当于加水将硫酸稀释,所以氢离子浓度减小,反应速率减慢,故A正确;选项B中加入氯化铜溶液,锌置换出铜,形成Cu―Zn原电池,使反应速率更快,B不正确;选项C主事先在硫酸溶液中加入等体积的NaCl溶液,相当于加水将硫酸稀释,所以氢离子浓度减小,反应速率减慢,故C正确。
考点:考查影响化学反应速率因素的有关实验探究
点评:该题是中等难度的试题,也是高考中的常见题型,有利于培养学生规范严谨的实验设计能力,有助于提升学生的学科素养,提高学生的应试能力。该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:困难
|