微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 空气中含量最多的元素与原子核外电子数最少的元素组成的简单物质的电子式???????,该分子属于???????????(填“极性”或“非极性”)分子。
参考答案: 本题解析:
本题解析:
试题分析:空气中含量最多的元素与原子核外电子数最少的元素分别是N和H,二者组成的简单物质是氨气,含有极性键的共价化合物,电子式是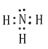 。由于氨气是三角锥形结构,所以氨气是极性分子。
。由于氨气是三角锥形结构,所以氨气是极性分子。
点评:该题的关键是准确判断出元素的名称,难度不大,侧重对学生基础知识对巩固和检验。
本题难度:一般
2、选择题 甲烷分子的结构式
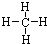
,关于其结构叙述中正确的是( )
A.甲烷分子是正方形结构
B.甲烷分子中4个碳氢键不相同
C.甲烷分子的四个键完全相同
D.甲烷分子的四个键完全不相同
参考答案:A.甲烷的结构为正四面体构型,故A错误;
B.甲烷分子
本题解析:
本题难度:简单
3、填空题 (1)肼(N2H4)是火箭发动机的燃料,它与N2O4反应时,N2O4为氧化剂,生成氮气和水蒸气。
已知:N2(g)+2O2(g)===N2O4(g) ΔH=+8.7 kJ/mol,N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH=-534.0 kJ/mol, 则表示肼跟N2O4反应的热化学方程式
(2)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g)  CH3OH(g) ΔH=-90.7 kJ・mol-1
CH3OH(g) ΔH=-90.7 kJ・mol-1
2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ・mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ・mol-1
CO(g)+H2O(g)  CO2(g)+H2(g)[来源:学科网ZXXK] ΔH=-41.2 kJ・mol-1
CO2(g)+H2(g)[来源:学科网ZXXK] ΔH=-41.2 kJ・mol-1
则CO2和氢气合成CH3OCH3(g)的热化学方程式为
______________________________________________________________________。
参考答案:(1) 2N2H4(g) + N2O4(g) = 3N2(g
本题解析:
试题解析:(1)根据盖斯定律,将方程式②×2-①得肼和N2O4反应的热化学方程式,2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) ΔH=" -1076.7" kJ/mol;(2)利用盖斯定律进行计算,将三个已知方程式分别变形为:2CO(g)+4H2(g)=2CH3OH(g)△H=-181.42kJ/mol,CH3OH(g=CH3OCH3(g)+H2O(g)△H="-23.5" kJ/mol,2CO2(g)+2H2(g)=2CO(g)+2H2O(g)△H=+82.4kJ/mol,三式相加得:
2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)△H=-122.5kJ/mol。
考点:盖斯定律的应用
本题难度:一般
4、填空题 (6分)在①Ar ②干冰③SiO2 ④NH4Cl ⑤K2S⑥金刚石六种物质,按下列要求回答(填序号)
⑴只存在共价键的是???????,既存在离子键,又存在共价键的是???????;
⑵熔化时不需破坏化学键的是??????????,熔化时需要破坏共价键的是???????;
⑶写出①的电子式是????????,④的电子式是???????。
参考答案:⑴③⑥;④??⑵?①②?;③⑥;⑶① 本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。据此可知①中没有化学键,熔化破坏的是分子间作用力。②中含有极性键,熔化破坏的是分子间作用力。③中含有极性键,熔化破坏的是极性键。④含有离子键和极性键,熔化破坏的是离子键。⑤含有离子键,熔化破坏的是离子键。⑥含有非极性键,熔化破坏的是非极性键。Ar的电子式为
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。据此可知①中没有化学键,熔化破坏的是分子间作用力。②中含有极性键,熔化破坏的是分子间作用力。③中含有极性键,熔化破坏的是极性键。④含有离子键和极性键,熔化破坏的是离子键。⑤含有离子键,熔化破坏的是离子键。⑥含有非极性键,熔化破坏的是非极性键。Ar的电子式为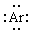 本题难度:一般
本题难度:一般
5、选择题 已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g) △H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l) △H4;
则△H四者的关系中正确的是
A.△H1>△H2>△H3>△H4
B.△H4>△H2>△H3>△H1
C.△H3>△H4>△H1>△H2
D.△H4>△H3>△H2>△H1
参考答案:C
本题解析:
试题分析:H2S完全燃烧生成液体水时放出的热量最多,但放热越多,△H越小,因此最小△H2,其次是△H1;H2S不完全燃烧放出的热量少,其中生成气态水放热最少,所以△H3最大,其次是△H3,因此△H四者的关系中正确的是△H3>△H4>△H1>△H2,答案选C。
考点:考查反应热大小比较的判断
本题难度:一般