��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp��4��10��10������˵������ȷ����
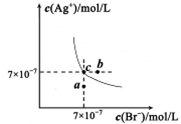
A����t��ʱ��AgBr��KspΪ4.9��10��13
B����AgBr������Һ�м���NaBr���壬��ʹ��Һ��c�㵽b��
C��ͼ��a���Ӧ����AgBr�IJ�������Һ
D����t��ʱ��AgCl(s)��Br��(aq)  AgBr(s)��Cl��(aq)ƽ�ⳣ��K��816
AgBr(s)��Cl��(aq)ƽ�ⳣ��K��816
�ο��𰸣�B
�������������ͼ��c���c(Ag��)��c(Br��)�ɵã����¶���AgBr��KspΪ4.9��10��13��A��ȷ����AgBr������Һ�м���NaBr�����c(Br��)�������ܽ�ƽ�������ƶ���c(Ag��)��С��ƽ������������ϣ�B������a��ʱQc��Ksp����ΪAgBr�IJ�������Һ��C��ȷ��ѡ��D�� ���������ݵ�K��816��
���������ݵ�K��816��
�����Ѷȣ�һ��
2��ѡ���� ��֪298 Kʱ��Mg(OH)2���ܶȻ�����Ksp��5.6��10��12��ȡ������MgCl2��Һ������һ�������ռ���Һ�ﵽ�����ܽ�ƽ�⣬���pH��13��������˵������ȷ����(? )
A��������Һ�е�c(H��)��1.0��10��13mol��L��1
B��������Һ����ˮ���������c(OH��)��1.0��10��13 mol��L��1
C�����ӵ��ռ���ҺpH��13
D��������Һ�е�c(Mg2��)��5.6��10��10 mol��L��1
�ο��𰸣�C
�������������һ�������ռ���Һ���pH��13���������ռ���Һ��pH����13����C�����A��B��D����ȷ��
�����Ѷȣ�һ��
3��ѡ���� ��3�֣�����˵������ȷ����__________��
A�����ʵ��ܽ�����¶ȵ����߶����ӣ������ʵ��ܽⶼ�����ȵģ�
B������Al(OH)3(s)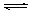 Al(OH)3(aq)
Al(OH)3(aq) 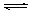 Al3+��3OH-��ǰ��Ϊ�ܽ�ƽ�⣬����Ϊ����ƽ�⣻
Al3+��3OH-��ǰ��Ϊ�ܽ�ƽ�⣬����Ϊ����ƽ�⣻
C����ȥ��Һ�е�Mg2+����OH-����Mg2+����CO32-Ч���ã�˵��Mg(OH)2���ܽ�ȱ�MgCO3��
D��������Ӧ�г��ӹ����ij���������Ŀ����ʹ������ȫ��
�ο��𰸣�(3��)? A C
���������A���������������ܽ��ų�������B��ȷ��Al(OH)3(s)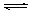 Al(OH)3(aq)
Al(OH)3(aq) 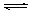 ?Al3+��3OH-��ǰ��Ϊ��
?Al3+��3OH-��ǰ��Ϊ��
�����Ѷȣ�һ��
4������� ��14�֣��±��Dz�ͬ�¶���ˮ�����ӻ����ݣ�
�¶�/��
| 25
| t1
| t2
|
Kw/ mol2��L-2
| 1��10-14
| a
| 1��10-12
�Իش����¼������⣺
��1����25< t1< t2����a??????1��10-14���<������>����=�������ɴ��жϵ������ǣ�
???????????????????????????????????????????????????????????
��2����25 ���£�pH=10��NaOH��Һ�У�ˮ���������[OH-]Ϊ��?????????
��3����ij�¶��£���ˮ��c(H+) = 5��10-7 mol��L-1�����ʱ��ˮ�е�c(OH-)=_______________�����¶Ȳ��䣬����ϡ����ʹc(H+)=5.0��10-3 mol��L-1����c(OH-)=_______________��
�ο��𰸣���1����??ˮ�ĵ���Ϊ���ȷ�Ӧ�������¶ȣ�ƽ����������Ӧ����
�������������ˮ�ĵ���
��1��ˮ�ĵ���ƽ��Ϊ��H2O H����OH�����������ȷ�Ӧ�������¶ȣ�ƽ����������Ӧ�����ƶ���[H+]����[OH-]����Kw =c(H+)c(OH-)��Kw���� H����OH�����������ȷ�Ӧ�������¶ȣ�ƽ����������Ӧ�����ƶ���[H+]����[OH-]����Kw =c(H+)c(OH-)��Kw����
��2���ڼ���Һ�У�H+ȫ��������ˮ�ĵ��룬��Ũ��Ϊ10-10 mol��L-1
��3����ˮ�У�c(H+) =c(OH-)
�����Ѷȣ���
5��ѡ���� һ���¶��£�����������ȷ����
A����AgClˮ��Һ�м��뱥��NaCl��Һ��c(Cl-)����AgCl���ܶȻ�����
B�������ܵ���ʷ��봿ˮ�У��ܽ��ƽ��ʱ����������ӵ�Ũ�ȵij˻����Ǹ����ʵ��ܶȻ�
C������AgCl�������Һ�м���������ˮʹAgCl�ܽ⣬���´ﵽƽ��ʱ��AgCl���ܶȻ����䣬���ܽ��Ҳ����
D��AgCl��Ksp��1.8��10��10mol2��L��2�������κκ�AgCl�������Һ�У�c(Ag��)��c(Cl��)��Ag����Cl��Ũ�ȵij˻�����1.8��10��10mol2��L��2
�ο��𰸣�C
���������
����������ܶȻ�ֻ���¶��йأ���Ũ���أ�A�������ܵ���ʷ��봿ˮ�У��ܽ��ƽ��ʱ����������ӵ�Ũ�ȵ�ϵ���η��ij˻����Ǹ����ʵ��ܶȻ���B����ֻ����AgCl������Һ�в��У�c(Ag��)��c(Cl��)�������AgCl������Һ���뺬��Cl-��Ag+�����ʣ�c(Ag��)��c(Cl��)��D����ѡC��
�������ܶȻ������¶��й�ϵ������Һ��Ũ���أ��¶ȱ��ܶȻ��ı䡣
�����Ѷȣ�һ��
|